암 네트워크 진화와 제어: 불리언 관점
초록
본 논문은 단백질 상호작용과 단계별 유전자 발현 데이터를 통합해 불리언 네트워크를 구성하고, 이를 ‘암 상태 공간’으로 모델링한다. BoolSpace라는 프레임워크를 통해 정상·종양 및 진행 단계 간의 네트워크 재배선(편집)과 유전자 플립을 분석하고, 전이 과정에서 핵심 역할을 하는 최소 유전자 집합(MIN‑FLIP)을 효율적으로 탐색한다. 췌장·유방암 및 척수 손상 모델에 적용한 결과, 세린/트레오닌 키나아제가 빈번히 플립되며 초기와 후기 단계에서 서로 다른 유전자 집합이 관여함을 확인하였다.
상세 분석
본 연구는 암 진행을 동적인 시스템으로 바라보아, 기존의 정적 네트워크 분석을 넘어 시간에 따라 변하는 ‘상태 전이’를 정량화한다는 점에서 혁신적이다. 먼저, 저자들은 Biogrid에서 추출한 29,600개의 고품질 물리적 상호작용을 백본으로 삼고, 각 단계(정상, 종양, 진행 단계)의 다중 샘플 유전자 발현 데이터를 이용해 상호작용 쌍의 피어슨 상관계수를 계산한다. 상관계수가 양(≥δ)이면 NOT‑XOR(¯⊗), 음(≤‑δ)이면 XOR(⊗) 형태의 불리언 절을 부여함으로써, 물리적 상호작용이 실제 코-발현에 의해 ‘활성화’ 혹은 ‘억제’되는지를 논리식으로 표현한다. 이렇게 구성된 조건부 불리언 네트워크 BΩ는 각 유전자를 0/1 변수로, 각 상호작용을 논리식으로 매핑한다.
전이 모델링에서는 두 연속 단계 Ω와 Ψ 사이의 상관 변화에 따라 상호작용을 ‘손실’, ‘획득’, ‘전환(toggling)’으로 구분한다. 전환은 양의 코‑발현이 음으로, 혹은 그 반대로 바뀔 때 발생하며, 이는 논리식의 ¯⊗↔⊗ 변환으로 구현된다. 이러한 편집 집합 EΩΨ가 주어지면, 기존 만족 할당 B(BΩ)를 유지하면서 새 네트워크를 만족시키기 위해 최소한의 유전자 플립 집합 V0Ω를 찾는 문제가 MIN‑FLIP이다.
알고리즘적 측면에서 저자들은 MIN‑FLIP을 MIN‑ONES‑2SAT 문제와 동치임을 보이고, 일반 경우는 NP‑complete이지만, 플립 수 k를 파라미터로 두는 고정‑파라미터 트랙터블(FPT) 접근을 제시한다. 구체적으로, 각 유전자의 인접 상호작용을 SAT/UNSAT으로 분류하고, k 이하의 플립을 탐색하는 Branch‑and‑Bound 방식으로 O(f(k)·n^c) 시간 복잡도를 달성한다. 이는 실제 데이터에서 플립 수가 비교적 작다는 가정 하에 실용적인 해결책을 제공한다.
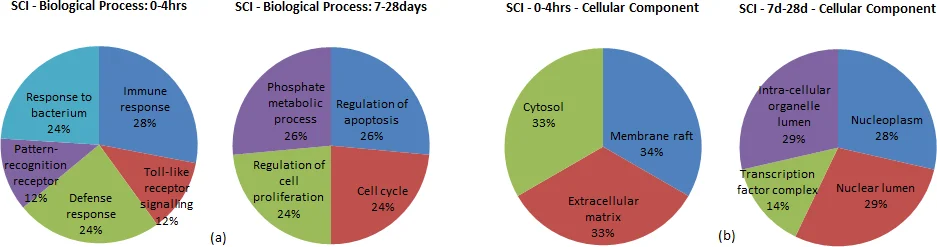
실험에서는 췌장암(PDAC)과 유방암, 그리고 라트 모델의 척수 손상 데이터를 적용하였다. 코‑발현 네트워크 분석 결과, 종양에서는 8,701개의 고상관 상호작용이 소실되고, 특정 상호작용(RBPMS‑RHOXF2, SMN1‑TMSB4X)에서 극단적인 ‘점프’가 관찰되었다. MIN‑FLIP 결과, 초기 단계에서는 세린/트레오닌 키나아제(예: CDK1, MAPK1)와 같은 스위치 역할 유전자가 주로 플립되었으며, 후기 단계에서는 DNA 복구·세포주기 억제와 관련된 유전자(예: ATM, BRCA1)가 새롭게 등장한다. 이는 암이 진행될수록 ‘배턴을 넘기는’ 메커니즘, 즉 서로 다른 기능군의 유전자가 순차적으로 핵심 역할을 담당한다는 가설을 뒷받침한다.
또한, 전이 과정에서 핵심 경로(세포주기, DNA 손상 복구)의 재배선이 빈번히 일어나며, 이는 기존 표적 치료가 특정 단계에만 효과적인 이유를 설명한다. 저자들은 이러한 결과를 토대로, 모든 단계에서 공통적으로 관여하거나 단계별로 교차하는 유전자들의 ‘커버 세트’를 목표로 하는 복합 치료 전략을 제안한다.
전반적으로 BoolSpace는 불리언 만족도와 네트워크 편집을 결합한 새로운 정량적 프레임워크를 제공하며, 암 진행의 동적 특성을 정밀하게 모델링하고, 치료 표적 발굴에 실용적인 인사이트를 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기