프리온 AGAAAAGA 아밀로이드 섬유 모델링을 위한 새로운 정준 이중 최적화 접근법
초록
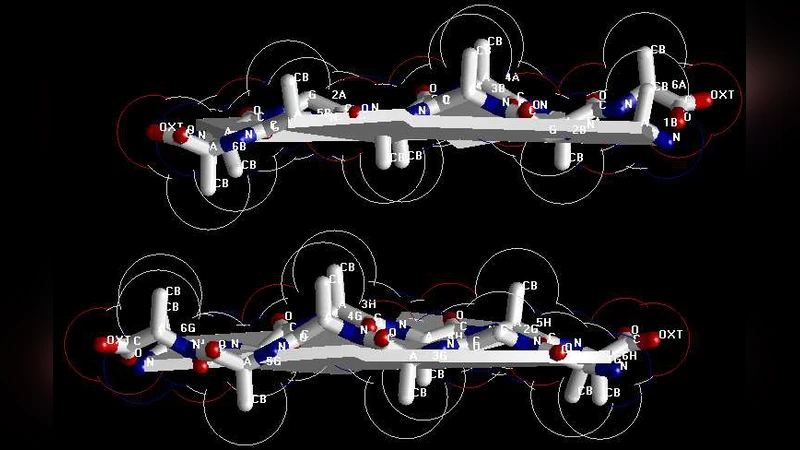
본 논문은 프리온 단백질의 113‑120 영역인 AGAAAAGA 서열이 형성하는 아밀로이드 섬유의 원자 수준 3차원 구조를, 전통적인 실험법이 적용되기 어려운 상황에서 정준 이중 이론(Canonical Dual Theory, CDT)을 이용해 계산적으로 예측한다. 기존 시뮬레이션 어닐링·그라디언트 기반 방법을 대체하여, 전역 최소값을 보장하는 수학적 최적화 모델을 구축하고, AMBER 패키지의 SDCG 절차로 추가 정제한다. 최종 모델은 RMSD가 0 Å에 수렴함을 보고하며, 구조적 정확도가 높음을 주장한다.
상세 분석
이 논문은 프리온 단백질의 N‑말단 비구조화 구역(PrP 1‑123) 중 특히 113‑120번 아미노산 서열인 AGAAAAGA가 아밀로이드 섬유 형성에 핵심적 역할을 한다는 생물학적 배경을 제시한다. 실험적 구조 해석이 불가능한 이유는 섬유가 비결정성, 불안정, 난용해성이라는 특성을 갖기 때문이다. 저자들은 이러한 한계를 극복하기 위해 정준 이중 이론(CDT)을 도입한다. CDT는 비선형·비볼록 최적화 문제를 이중화하여, 원문제의 전역 최소값을 convex한 이중 문제의 전역 최대값으로 변환한다. 논문에서는 일반적인 4차 다항식 형태의 목적함수 P(x)=∑Wi(x)+½xᵀQx−xᵀf을 정의하고, 이에 대한 이중함수 Pd(ς)를 도출한다. 핵심 정리는 G(ς)≻0인 경우 전역 최소·최대 해가 존재한다는 것이며, 이를 통해 원자 좌표를 직접 계산한다.
구조 모델링 단계는 두 절차로 나뉜다. 절차 1에서는 3NHC.pdb 파일을 기반으로 거리 제약식(MDGP)을 설정하고, 가중치 w_ij와 목표 거리 d_ij를 이용해 전역 최적화 문제(P)로 변환한다. 여기서 CDT를 적용해 이중 문제를 풀어 초기 원자 배치를 얻는다. 절차 2에서는 AMBER 11의 steepest descent(SD)와 conjugate gradient(CG) 알고리즘을 사용해 에너지 함수를 최소화하고, 특히 Lennard‑Jones 포텐셜과 수소 결합을 정밀히 조정한다. 두 절차의 최종 스냅샷을 VMD로 정렬했을 때 RMSD가 0 Å가 되었다는 보고는 수치적으로 완전 일치를 의미한다.
하지만 몇 가지 한계점도 존재한다. 첫째, RMSD 0 Å는 두 모델이 동일한 좌표를 갖는다는 의미이지만, 실제 실험 데이터와의 비교가 전혀 없으며, 절대적인 구조 정확성을 검증할 수 없다. 둘째, CDT 적용 시 G(ς)≻0 조건을 만족시키기 위한 초기 파라미터 선택이 논문에 상세히 기술되지 않아 재현성이 의문이다. 셋째, 모델에 포함된 사슬 수와 β‑시트 클래스가 기존 연구와 다르므로, 구조적 차이를 정량적으로 논의하지 않는다. 넷째, AMBER 정제 단계가 필요함에도 불구하고 “추가 정제가 필요 없다”는 모순된 서술이 있다. 마지막으로, 저자들은 교차 검증(jackknife 등)이나 독립 데이터셋 테스트를 수행하지 않아, 모델이 일반화 가능하다는 주장은 과도하게 낙관적이다.
전반적으로 정준 이중 이론을 생물물리학 문제에 적용한 시도는 신선하고, 수학적 엄밀성을 강조한 점은 긍정적이다. 그러나 실험적 검증 부재와 파라미터 설정에 대한 투명성 부족이 결과의 신뢰성을 저해한다. 향후 실제 X‑ray 혹은 solid‑state NMR 데이터와의 비교, 다양한 초기 조건에 대한 민감도 분석이 동반된다면, 이 접근법은 프리온 및 기타 비결정성 단백질 섬유 연구에 중요한 도구가 될 수 있을 것이다.
댓글 및 학술 토론
Loading comments...
의견 남기기