인플루엔자 A형 HA 유전자 진화 지도화: ISSCOR‑PCA 접근법
초록
**
본 논문은 인플루엔자 A형 바이러스의 혈구응집소(Hemagglutinin, HA) 유전자를 대상으로 ISSCOR(동일코돈 무작위 교체) 방법과 주성분 분석(PCA)을 결합해 서열 간의 순서 변이(코돈 순서 편차)를 정량화하였다. 9,131개의 HA 서열을 분석한 결과, HA‑1 도메인의 코돈 순서가 시간에 따라 뚜렷한 군집 변화를 보이며, H3N2는 조류→돼지→인간 순으로 진화하는 반면, 2009년 팬데믹 H1N1은 역전된 전이 양상을 나타냈다. 이러한 ISSCOR‑PCA 매핑은 대규모 유전체 데이터에서 빠른 트렌드 파악과 신종 변이 감지를 위한 유용한 도구임을 제시한다.
**
상세 분석
**
이 연구는 기존의 코돈 사용 빈도 분석을 넘어, 동일한 아미노산을 코딩하면서도 코돈 순서가 어떻게 재배열되는지를 탐구한다는 점에서 독창적이다. ISSCOR은 Monte‑Carlo 기반으로 원본 서열과 동일한 아미노산 서열을 유지하면서 무작위로 동의코돈을 교체한다. 이렇게 생성된 N개의 가상 서열 집합에 대해 각 코돈‑쌍(코돈‑스페이서 길이 λ) 발생 빈도를 행렬 Oλ로 기록하고, 원본 서열의 실제 빈도와 무작위 집합 평균·표준편차를 이용해 편차(Txx) 값을 산출한다. 편차는 정규화된 Z‑score와 유사하게 해석되며, 코돈 순서가 무작위 기대값에서 얼마나 벗어나는지를 정량화한다.
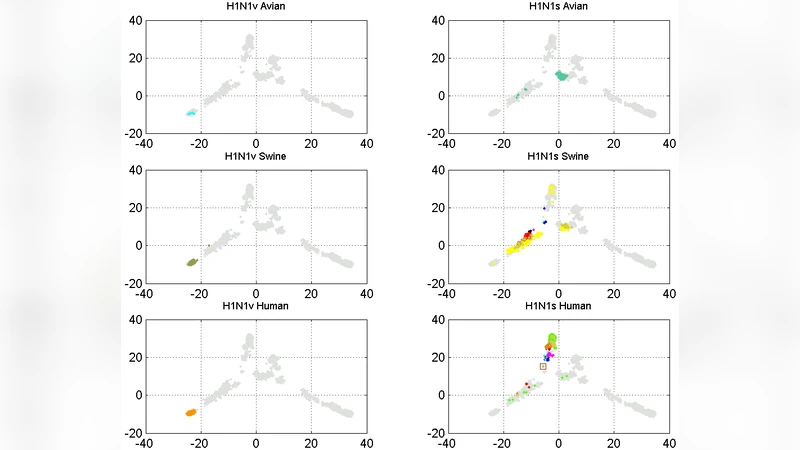
다음 단계에서는 9,131개의 HA 서열에 대해 λ=0~16까지의 편차를 모두 계산해 2,448차원의 특성 벡터(MA)를 구성하고, PCA를 적용했다. PC‑1이 전체 변동의 45.4%를, PC‑2가 18.3%를 설명함으로써 두 축만으로도 서열 간의 주요 차이를 시각화할 수 있었다. 색상과 호스트 구분을 통해 각 서브타입(H1N1, H3N2, H5N1 등) 및 숙주(조류, 인간, 돼지, 페럿)의 군집이 명확히 드러났으며, 특히 H3N2는 조류→돼지→인간 순으로 연속적인 이동 경로를 보였다. 반면 2009년 팬데믹 H1N1은 조류에서 인간으로 직접 전이된 사례가 소수 존재함을 확인했는데, 이는 기존의 “조류→돼지→인간” 전이 모델에 예외적인 경로가 존재함을 시사한다.
또한, 전체 데이터가 삼각형 형태의 분포를 이루며, 가장 오래된 1918년 H1N1이 상단에, 최신 H3N2가 오른쪽 하단에, 2009년 팬데믹 H1N1이 왼쪽 하단에 위치한다는 점은 시간에 따른 진화 흐름을 직관적으로 보여준다. 이러한 시각화는 전통적인 계통수 기반 분석과 달리 연속적인 변이 흐름을 한눈에 파악하게 해준다.
하지만 몇 가지 한계도 존재한다. 첫째, ISSCOR은 코돈 순서만을 무작위화하므로, 실제 바이러스 복제 과정에서 발생하는 선택압(예: RNA 구조, 번역 효율 등)을 완전히 반영하지 못한다. 둘째, λ값을 늘릴수록 희소성이 감소하지만, 고차원 n‑gram(λ>8)에서는 통계적 신뢰도가 떨어질 수 있다. 셋째, PCA는 선형 변동만을 포착하므로 비선형 관계가 존재할 경우 정보 손실이 발생한다. 마지막으로, 데이터베이스에 포함된 서열이 지역·시기별 편향을 가질 수 있어, 관측된 군집이 실제 전이 경로와 완전히 일치하지 않을 가능성이 있다.
그럼에도 불구하고, ISSCOR‑PCA는 대규모 유전체 데이터에서 코돈 순서의 미세한 변화를 정량화하고, 시계열·공간적 트렌드를 시각화하는 강력한 도구로 평가된다. 향후에는 다른 바이러스(예: 코로나바이러스)나 박테리아 유전체에도 적용해 조기 경보 시스템을 구축할 수 있을 것으로 기대된다.
**
댓글 및 학술 토론
Loading comments...
의견 남기기