히스토마크 전파 모델로 보는 인간 염색질 이질성 재현
** 본 연구는 히스톤 H3K9me(이질염색질)와 H3K4me·아세틸(활성염색질) 마크가 DNA 상에서 서로 반대되는 대규모 도메인을 형성한다는 실험적 증거를 바탕으로, ‘핵형성‑전파‑경쟁‑소거’ 네 가지 확률적 과정을 포함한 최소한의 컴퓨터 모델을 구축하였다. 모델은 인간 1번 염색체 전체에 대해 시뮬레이션을 수행하고, CD4⁺ T 세포와 HeLa 세포의 ChIP‑seq 데이터와 비교했을 때 도메인 크기·위치·경계 형태가 높은 일치를 보였…
저자: Veit Schw"ammle, Ole N{o}rregaard Jensen
**
본 논문은 히스톤 변형이 염색질 구조와 전사 조절에 미치는 영향을 대규모 도메인 수준에서 이해하고자 하는 목표로 시작한다. 서론에서는 히스톤 옥틸레이트, 메틸레이션, 인산화 등 다양한 포스트트랜슬레이셔널 변형이 유전자의 활성·억제에 어떻게 기여하는지를 개괄하고, 특히 H3K9me2/3(이질)와 H3K4me2/3·아세틸(활성) 마크가 서로 반대되는 영역을 형성한다는 기존 연구들을 인용한다. 이어서 ‘핵형성(Nucleation)’, ‘전파(Propagation)’, ‘경쟁(Competition)’, ‘소거(Deletion)’ 네 가지 핵심 메커니즘을 제시한다.
핵형성 부위는 Alu·SINE(이질)와 CpG 섬(활성) 등 특정 DNA 서열로 정의되며, 이들 서열이 히스톤 변형을 직접 시작하는 ‘시드’ 역할을 한다고 가정한다. 전파는 인접 nucleosome 사이에서 마크가 복제되는 과정으로, 확률 pₛ₁(이질)·pₛ₂(활성)로 모델링한다. 경쟁은 동일 nucleosome이 두 종류의 마크를 동시에 가질 수 없다는 제약을 의미하며, 충돌 시 기존 마크가 소거되고 새로운 마크가 자리 잡는다. 소거는 무작위로 마크가 사라지는 과정으로, 히스톤 교체·디메틸화·디아세틸화 등을 대변한다.
이러한 규칙을 바탕으로 저자들은 전체 인간 1번 염색체(≈250 Mbp)를 1 kb 격자로 이산화하고, 각 격자에 대해 시간 단계별 확률적 업데이트를 수행하는 Monte‑Carlo 시뮬레이션을 구현한다. 모델은 DNA 복제·히스톤 재배열을 무시하고, 오직 인접 상호작용만을 고려한다. 파라미터는 실험 데이터와의 최적화 과정을 통해 설정되었으며, 핵형성 부위의 밀도와 전파 속도 비율이 도메인 경계와 전체 염색질 상태를 결정한다는 핵심 결과를 도출한다.
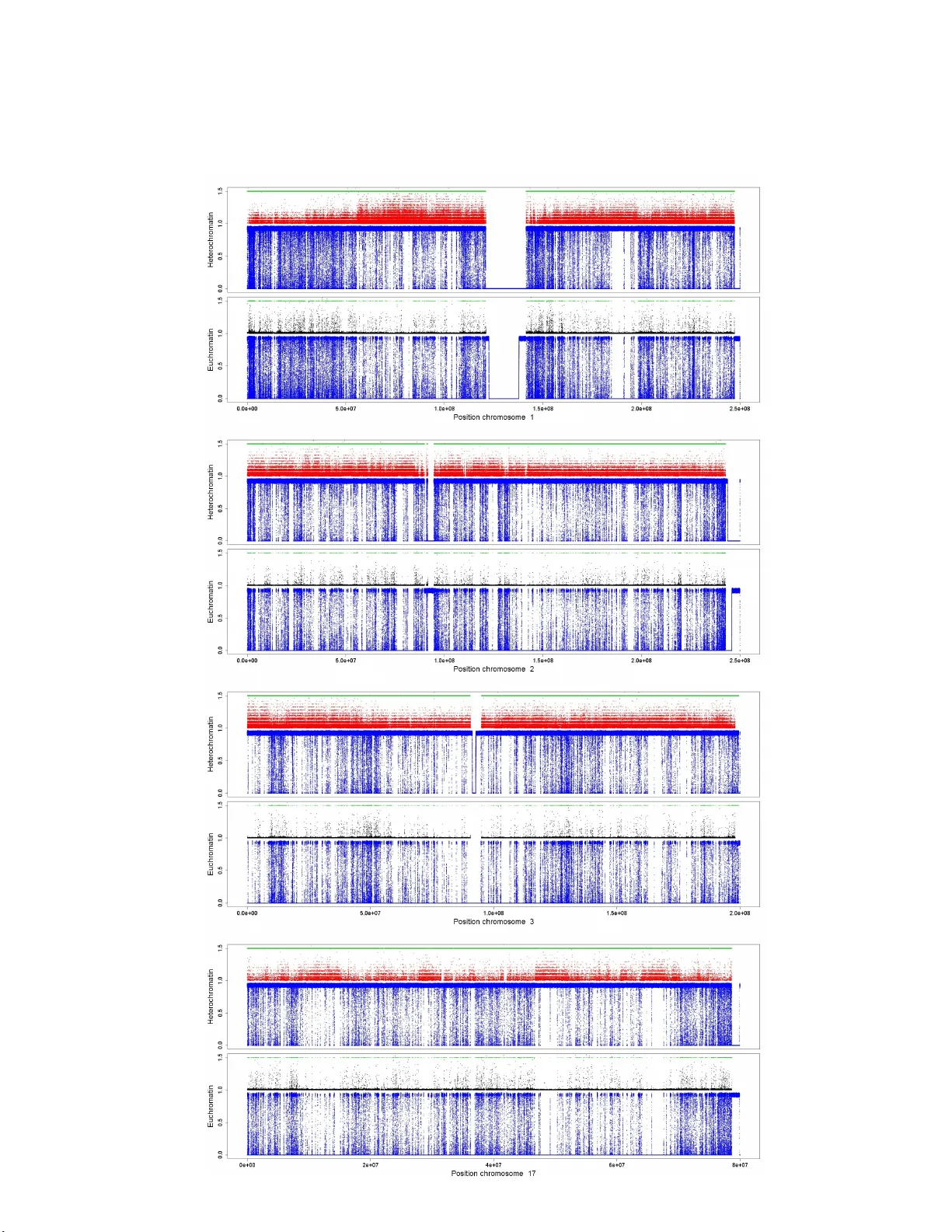
실험 검증을 위해 저자들은 인간 CD4⁺ T 세포와 HeLa 세포에서 공개된 ChIP‑seq 데이터를 활용하였다. CCAT(v3.0) 툴을 이용해 H3K9me2/3, H3K4me2/3, H3K14/18/23ac 등의 점수를 100 kb 구간으로 집계한 결과, 이질 마크와 활성 마크가 거의 완전한 반상관을 보이며, 각 마크가 형성하는 도메인의 평균 크기가 수천 개 히스톤(≈100 kb) 수준임을 확인했다. 이러한 실험적 도메인 구조와 시뮬레이션 결과가 시각적으로도 일치했으며, 특히 알루와 CpG 섬이 위치한 구간에서 마크 전환이 급격히 일어나는 현상이 모델에 의해 재현되었다.
파라미터 스캔 실험에서는 (1) 핵형성 부위가 희소한 구간에서는 전파가 자연스럽게 멈추어 ‘바리어’가 형성되고, (2) 전파 속도 pₛ₁이 pₛ₂보다 크게 증가하면 전체 염색체가 이질 상태로 전환되는 ‘전이 현상’이 관찰되었다. 또한, 인위적으로 핵형성 부위의 위치를 이동시키면 해당 구역의 전사 활성도가 예측대로 상승·감소함을 확인함으로써, 핵형성 부위 분포가 전사 프로그램을 전역적으로 조절한다는 가설을 실험적으로 뒷받침했다.
논의에서는 모델의 장점과 한계를 짚는다. 장점으로는 (i) 복잡한 히스톤 상호작용 네트워크를 최소한의 확률 규칙으로 축소했음, (ii) 전사 활성·억제의 전역적 패턴을 정량적으로 예측할 수 있음, (iii) 핵형성 부위와 전파 속도 조절을 통해 특정 유전자군의 발현을 설계적으로 바꿀 수 있는 가능성을 제시함을 들었다. 한계로는 (i) DNA 복제·히스톤 교체 주기의 동적 효과를 무시했음, (ii) 3차원 염색질 구조에 의한 장거리 상호작용을 모델에 포함하지 않았음, (iii) H3K27me3·Polycomb 등 다른 억제 마크를 고려하지 않아 실제 세포에서 나타나는 복합적인 에피제네틱 스위치를 완전히 설명하지 못함을 인정한다.
결론적으로, 이 연구는 히스톤 마크 전파와 경쟁을 기반으로 한 최소 모델이 인간 염색체 전반에 걸친 이질·활성 도메인 형성을 성공적으로 재현함을 보이며, 핵형성 부위의 분포와 전파 속도가 전사 프로그램을 전역적으로 제어한다는 새로운 통찰을 제공한다. 향후 연구에서는 복제 주기, 3D 구조, 추가적인 히스톤 변형을 통합한 확장 모델이 필요하다는 점을 제시한다.
**
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기