막 단백질의 방향성 상호작용과 협동성
초록
이 연구는 막 단백질의 형태가 주변 지질 이중층의 탄성 변형을 통해 발생하는 상호작용에 미치는 영향을 분석한다. 메카노센시티브 이온 채널을 모델로 삼아, 단백질의 방향과 형상이 탄성 상호작용의 부호와 강도를 결정하고, 이에 따라 협동 개폐 곡선이 달라짐을 보여준다. 결과는 고밀도 막에서 단백질의 구조·배열·기능이 어떻게 조절되는지를 예측한다.
상세 분석
본 논문은 막 단백질이 삽입된 지질 이중층을 연속체 탄성체로 모델링하고, 단백질 자체를 비구면(특히 타원형 또는 원추형) 형태의 삽입물로 가정함으로써, 단백질 간의 장거리 탄성 상호작용을 정량적으로 계산한다. 핵심은 두 단백질 사이의 거리와 상대적 회전각에 따라 발생하는 변형 에너지의 부호가 바뀔 수 있다는 점이다. 즉, 특정 방향에서는 서로를 끌어당겨 협동적인 개폐를 촉진하고, 반대 방향에서는 반발하여 개폐를 억제한다.
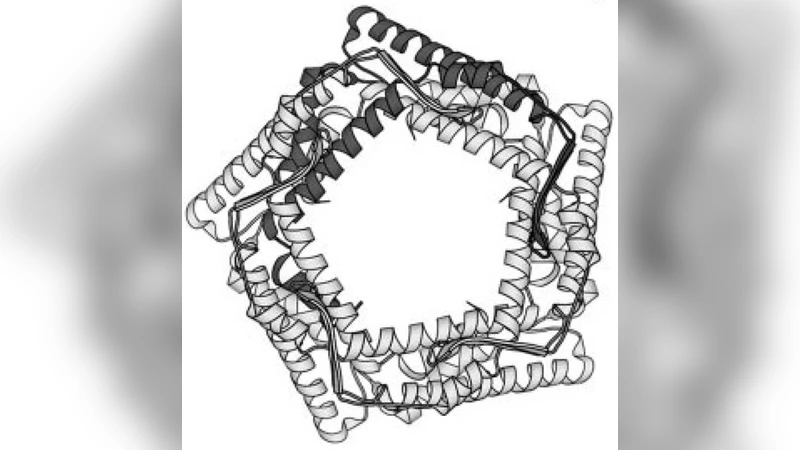
연구팀은 메카노센시티브 이온 채널(MSC)인 MscL과 MscS를 대표적인 실험 모델로 선택하였다. 이들 채널은 막에 가해지는 장력에 민감하게 반응해 개방되며, 구조적으로는 원통형(대칭)과 비대칭(비대칭적 트랜스메브레인 도메인) 두 종류가 존재한다. 논문은 고해상도 X‑ray 및 Cryo‑EM 구조 데이터를 바탕으로 각 채널의 단면 형상을 파라미터화하고, 이를 이용해 탄성 상호작용 포텐셜을 유도한다.
주요 발견은 다음과 같다.
- 형상 의존성: 원통형 대칭 단백질은 거리 의존적인 단순한 인력/반발 포텐셜을 보이지만, 비대칭 단백질은 회전각에 따라 부호가 바뀌는 복합 포텐셜을 나타낸다. 이는 비대칭 구조가 주변 막을 비등방성으로 변형시키기 때문이다.
- 협동 개폐 곡선: 두 채널이 일정 거리 이하에 위치하면, 동일한 방향(예: 동일한 회전각)에서는 개방 전압(또는 장력) 임계값이 낮아져 협동적 개방이 촉진된다. 반대로 반대 방향에서는 임계값이 상승해 억제 효과가 나타난다.
- 거리와 각도 임계값: 계산된 포텐셜을 바탕으로, 협동 효과가 유의미하게 나타나는 최대 거리(~10 nm)와 회전각 범위(~30°)를 제시한다. 이는 실제 세포막에서 단백질 밀도가 높은 영역(예: 박테리아의 세포벽 근처)에서 흔히 관찰될 수 있다.
- 예측 가능성: 제시된 모델은 단백질 변이(예: 도메인 삽입·삭제)나 지질 조성 변화(예: 포스포리피드 비율) 등에 대한 탄성 상호작용 변화를 정량적으로 예측한다. 실험적으로는 플루오레센스 FRET, 전기생리학적 파치 클램프, 혹은 고해상도 AFM을 이용해 검증 가능하다.
이러한 결과는 막 단백질이 단순히 독립적인 개별체가 아니라, 주변 막을 매개로 한 ‘기계적 네트워크’를 형성한다는 새로운 관점을 제공한다. 특히, 메카노센시티브 채널처럼 물리적 힘에 반응하는 단백질은 주변 단백질의 배향과 거리 배치를 통해 민감도가 조절될 수 있음을 시사한다. 이는 세포가 외부 자극에 대한 반응성을 미세하게 튜닝하는 메커니즘을 설명하는 데 기여한다.
댓글 및 학술 토론
Loading comments...
의견 남기기