Bcl‑2 패밀리와 MOMP 조절을 밝히는 불린 네트워크 모델
초록
본 연구는 Bcl‑2 패밀리 단백질 간 상호작용을 불린 네트워크로 구현하여 미토콘드리아 외막 투과(MOMP) 조절 메커니즘을 정량적으로 분석한다. 시뮬레이션 결과, 특정 항‑세포 사멸 단백질(Mcl‑1)의 지속적 활성화가 외부 자극과 무관하게 MOMP를 억제하는 ‘악성’ 상태를 만들 수 있음을 확인하였다. 또한 Bid와 Bim이 Bax·Bak 활성화에 필수적이며, 한 번 활성화된 효과기는 되돌릴 수 없는 특성을 보인다. Bcl‑w는 Bax 억제에 핵심적인 역할을 수행한다는 점도 밝혀졌다. 이러한 통찰은 항암제 설계 시 Bcl‑2 패밀리 표적 선택에 중요한 지침을 제공한다.
상세 분석
본 논문은 Bcl‑2 패밀리 단백질을 정점(node)으로, 서로 간의 억제·활성화 관계를 논리식(logic rule)으로 정의한 불린 네트워크 모델을 구축하였다. 각 정점은 ‘활성(1)’ 혹은 ‘비활성(0)’ 두 가지 상태만을 가질 수 있으며, 업데이트는 동기식(synchronous) 방식으로 진행되어 모든 정점이 동시에 현재 상태에 기반한 논리 함수를 적용받는다. 모델에는 14개의 주요 Bcl‑2 멤버(예: Bax, Bak, Bid, Bim, Mcl‑1, Bcl‑w 등)와 외부 사망 신호(Death) 및 생존 신호(Survival)와 같은 입력 노드가 포함된다. 논리식은 실험적으로 보고된 상호작용—예컨대, BH3‑only 단백질인 Bid와 Bim이 Bax·Bak을 직접 활성화하고, Mcl‑1·Bcl‑w·Bcl‑2·Bcl‑xL이 이를 억제한다—를 그대로 반영한다.
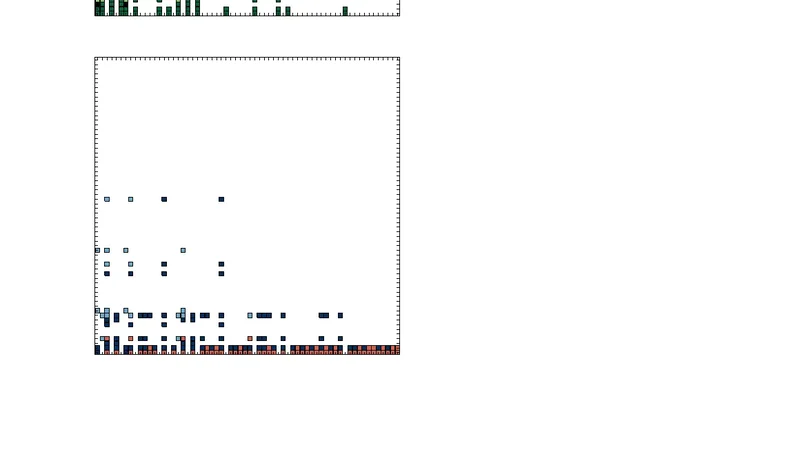
시뮬레이션은 모든 가능한 초기 상태(2^14 ≈ 16,384)와 다양한 입력 조합을 탐색함으로써 네트워크의 수렴점(attractor)을 도출하였다. 주요 결과는 두 종류의 고정점이 존재한다는 점이다. 하나는 ‘MOMP‑ON’ 상태로, Bax·Bak이 활성화되어 미토콘드리아 외막 투과가 일어나며, 다른 하나는 ‘MOMP‑OFF’ 상태로, 모든 효과기가 비활성화된 채 유지된다. 특히, Mcl‑1이 지속적으로 활성화된 경우 외부 Death 신호가 주어져도 네트워크는 ‘MOMP‑OFF’ 고정점에 머무르는 ‘악성’ 구성(configuration)이 발견되었다. 이는 Mcl‑1이 다른 항‑세포 사멸 단백질보다 우선적으로 Bax·Bak을 억제함을 시사한다.
또한, Bid와 Bim이 동시에 비활성화되면 Bax·Bak이 절대 활성화되지 못하고, 반대로 두 단백질이 활성화될 경우 일단 Bax·Bak이 켜진 뒤에는 논리식에 의해 자동으로 유지되는 ‘irreversible’ 특성이 나타난다. 이는 실제 세포에서 MOMP가 일단 발생하면 되돌릴 수 없는 ‘점프’ 현상을 모델링한 것으로 해석된다. Bcl‑w에 대한 분석에서는, Bcl‑w가 존재할 때 Bax의 활성화가 거의 차단되는 반면, Bak은 상대적으로 덜 억제되는 차별적 효과가 드러났다. 이러한 차이는 Bax와 Bak이 서로 다른 BH3‑only 단백질에 민감하게 반응한다는 기존 생화학적 보고와 일치한다.
모델의 제한점도 명시된다. 불린 접근은 정량적 농도 차이를 무시하고 이진 상태만을 고려하므로, 단백질 발현량의 미세한 변동이나 포스트트랜슬레이션 변형을 반영하기 어렵다. 또한, 동기식 업데이트는 실제 세포 내 비동기적 신호 전달을 단순화한다. 그럼에도 불구하고, 복잡한 상호작용을 직관적으로 시각화하고, 잠재적 ‘고정점’과 ‘전이 경로’를 체계적으로 탐색할 수 있다는 점에서 큰 장점이 있다. 이러한 모델링 결과는 항‑암제 개발 시 Mcl‑1 억제제와 Bcl‑w 표적화 전략이 MOMP 유도를 촉진할 수 있음을 뒷받침한다.
댓글 및 학술 토론
Loading comments...
의견 남기기