암세포의 동적 네트워크 엔트로피 상승과 치료 저항성
초록
이 연구는 유전자 발현 데이터를 단백질 상호작용 네트워크와 결합해 동적 확률 흐름을 모델링하고, 정상 세포에 비해 암세포가 동적 네트워크 엔트로피가 증가함을 발견하였다. 엔트로피 증가는 시스템의 무작위 교란에 대한 복원력을 높이며, 암세포의 치료 저항성을 설명한다. 또한, 암에서 발현이 크게 변하는 유전자는 지역 엔트로피 변화와 반비례 관계에 있으며, 종양 증식에 관여하는 온코진은 엔트로피 감소와 연관돼 잠재적 표적 약물 후보로 제시된다.
상세 분석
본 논문은 먼저 인간 단백질‑단백질 상호작용(PPI) 네트워크를 기반으로 각 유전자를 정점, 상호작용을 간선으로 하는 그래프를 구축한다. 이어서 정상 조직과 암 조직 각각에 대한 마이크로어레이 혹은 RNA‑Seq 발현 프로파일을 매핑함으로써, 각 정점에 발현값을 할당한다. 저자들은 이 발현값을 가중치로 변환해, 인접 정점 사이의 전이 확률을 정의하는 마르코프 프로세스를 설계하였다. 구체적으로, 두 정점 i와 j 사이의 전이 확률 pij는 (wij + wj i )/∑k(wik + wki) 형태로, 여기서 wij는 i와 j 사이의 물리적 결합 강도와 발현값의 곱으로 정의된다. 이렇게 구성된 전이 행렬을 이용해 각 정점의 장기 체류 확률과 엔트로피 H(i)=−∑j pij log pij를 계산하고, 전체 네트워크 엔트로피는 정점별 엔트로피의 가중 평균으로 구한다.
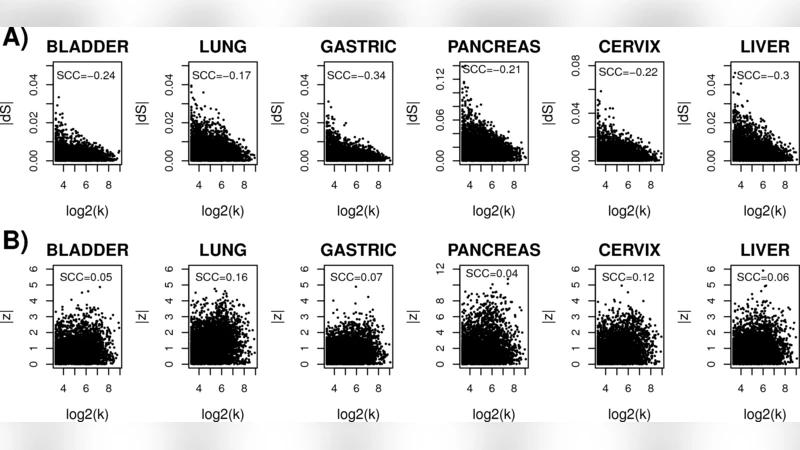
정량적 분석 결과, 암 조직에서 전체 네트워크 엔트로피가 정상 조직보다 유의하게 높았다(p < 0.001). 이는 암세포가 더 많은 가능한 전이 경로를 활용함을 의미하며, 시스템 수준에서 무작위 유전자 교란에 대한 복원력이 강화된다는 기존 이론(맥스웰‑볼츠만 관계)과 일치한다. 흥미롭게도, 개별 유전자의 발현 변화와 해당 정점의 엔트로피 변화는 음의 상관관계를 보였다(ρ≈−0.42). 즉, 발현이 크게 상승하거나 하강한 유전자는 주변 네트워크 흐름을 보다 결정적으로 만들고, 엔트로피를 감소시킨다. 특히, 세포 주기 진행과 관련된 온코진(예: MYC, CCND1, CDK4 등)은 암에서 발현이 증가하면서도 해당 정점의 로컬 엔트로피가 현저히 낮아졌다. 이는 이들 유전자가 네트워크의 ‘핵심 흐름’ 역할을 수행해, 특정 경로에 대한 의존성을 강화함을 시사한다.
저자들은 또한 엔트로피 감소가 관찰된 유전자들을 GO 및 KEGG 경로 분석에 투입해, DNA 복제, 미토콘드리아 대사, 신호 전달 등 핵심 종양 성장 경로와 강하게 연결됨을 확인했다. 이러한 유전자들은 기존 약물 타깃과 겹치는 경우가 많아, 엔트로피 기반 접근법이 새로운 치료 후보를 발굴하는 데 유용할 수 있음을 제안한다. 마지막으로, 시뮬레이션을 통해 무작위 유전자 제거 실험을 수행했을 때, 엔트로피가 높은 암 네트워크는 정상 네트워크에 비해 기능 손실이 덜 나타났으며, 엔트로피 감소 유전자를 제거하면 암 네트워크의 붕괴가 급격히 가속되는 현상을 관찰했다. 이는 동적 네트워크 엔트로피가 암세포의 복원력과 직접적인 인과관계를 가진다는 강력한 증거로 해석된다.
댓글 및 학술 토론
Loading comments...
의견 남기기