신장 배출이 가능한 금 나노클러스터의 독성 감소와 조직 분포
초록
본 연구는 BSA와 GSH로 보호된 금 나노클러스터의 24시간 및 28일 간 신장 배출, 조직 분포, 독성 반응을 비교하였다. GSH‑보호 나노클러스터는 24시간 내 36 %의 금이 신장을 통해 배출되고 28일 후 94 %가 대사된 반면, BSA‑보호 나노클러스터는 배출 효율이 1 %에 불과하고 5 % 미만만이 대사되었다. 초기 급성 염증과 신장 기능 손상은 두 종류 모두에서 나타났지만, GSH‑보호 클러스터는 28일 후 회복되었으며 BSA‑보호 클러스터는 지속적인 독성을 보였다.
상세 분석
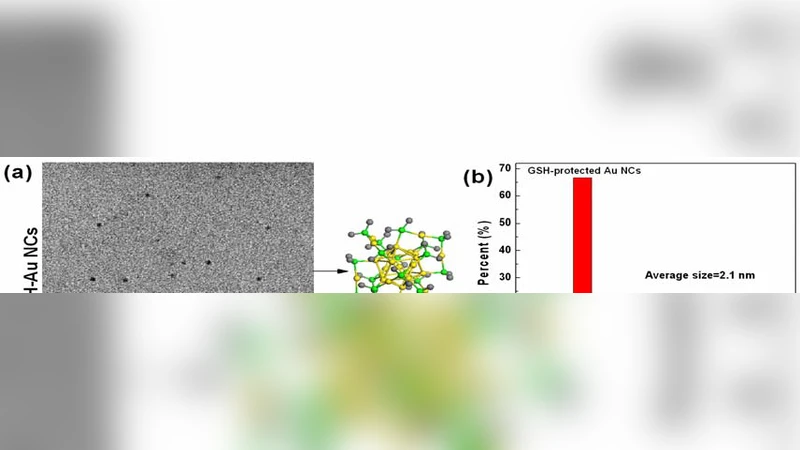
이 논문은 나노입자의 크기와 표면 리간드가 체내 운명에 미치는 영향을 정량적으로 규명한다는 점에서 의미가 크다. BSA‑보호 금 나노클러스터는 평균 직경이 5–8 nm 수준이지만, 혈액 내 단백질과 결합하면서 다중 나노입자 복합체를 형성해 실질적인 수치상 크기가 50 nm 이상으로 증가한다. 이는 사구체 여과막을 통과하지 못하게 하여 신장 배출이 거의 차단되고, 간·비장에 축적되어 장기 독성을 초래한다. 반면 GSH‑보호 나노클러스터는 2 nm 이하의 초소형 클러스터이며, 전하가 음전하를 띠어 혈장 단백질과의 비특이적 결합이 제한된다. 결과적으로 24 시간 내에 36 %가 소변으로 배출되고, 28일 후 전체 금의 94 %가 체외로 배출되었다는 데이터는 신장 배출이 가능한 나노클러스터 설계의 성공을 입증한다. 독성 측면에서는 24 시간 후 ALT, AST, BUN, CRE 수치가 상승해 급성 간·신 손상이 확인되었지만, GSH‑보호 클러스터는 면역세포 활성화 지표(CD68, CD86 등)가 정상 수준으로 회복된 반면, BSA‑보호 클러스터는 지속적인 염증 마커와 조직 섬유화가 관찰되었다. 이러한 차이는 나노클러스터가 체내에서 어떻게 “보이는가”(protein corona 형성)와 “배출되는가”(신장 투과성)에 따라 독성 프로파일이 급격히 달라짐을 보여준다. 또한, 저자들은 28일 장기 관찰을 통해 조직학적 회복 여부를 확인함으로써, 단기 독성 평가는 장기 안전성을 보장하지 못한다는 점을 강조한다. 연구 결과는 GSH‑보호 금 나노클러스터가 영상 및 약물 전달 플랫폼으로 적합함을 시사하고, BSA‑보호 클러스터는 오히려 간암 치료와 같이 의도적으로 간에 축적시키는 전략에 활용될 가능성을 제시한다. 향후 연구에서는 표면 리간드의 최적화와 크기 조절을 통해 배출 효율을 더욱 높이고, 면역 회피 메커니즘을 정밀히 규명함으로써 임상 전이 가능성을 확대해야 할 것이다.
댓글 및 학술 토론
Loading comments...
의견 남기기