테트라사이클린 기반 신약의 분류 체계와 구조‑활성 관계 종합 고찰
초록
**
본 논문은 기존 및 차세대 테트라사이클린(TC) 약물을 약물학적 구조를 기준으로 새롭게 분류하고, 항균·비항균 활성을 결정짓는 구조‑활성 관계(SAR)를 정리한다. 핵심은 4개의 고리와 C4 아미노기, C10‑C12 케톤‑엔올 구조 등 필수 기능군을 강조하고, 리포필리시티와 금속이온 킬레이트 특성이 활성을 조절한다는 점이다. 또한, 최신 합성계열(아미노메틸시클린, 글리실사이클린 등)과 비임상 데이터(LogP, 흡수율, 반감기 등)를 제시해 차세대 TC 설계에 실용적 지침을 제공한다.
**
상세 분석
**
논문은 크게 네 부분으로 구성된다. 첫째, 테트라사이클린의 역사적 분류(1세대 → 생합성, 2세대 → 반합성, 3세대 → 전합성)와 현재의 ‘글리실사이클린/아미노메틸시클린’ 등 새로운 계열을 통합한 체계적 분류 체계를 제시한다. 기존 분류는 약물의 제조 방식에만 초점을 맞추었으나, 저자는 구조적 변형(특히 D‑고리와 R4‑R6 치환)의 기능적 의미를 반영해 ‘항균·비항균·다중표적’ 3대 카테고리로 재구성한다.
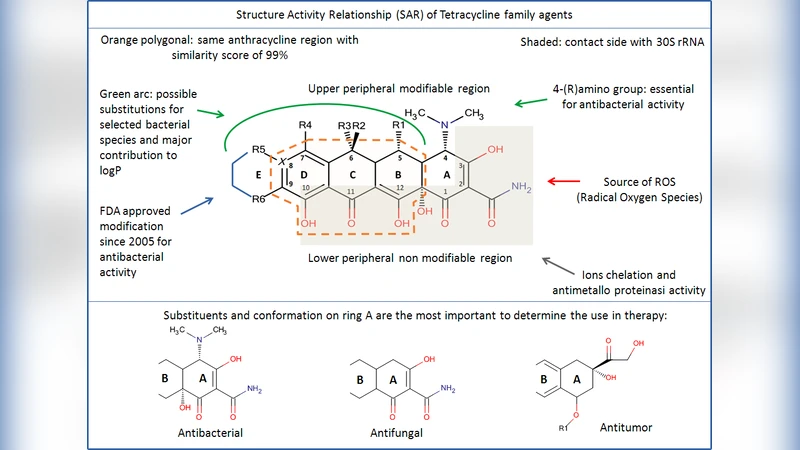
둘째, SAR 분석에서는 TC의 핵심 구조인 4개의 나프타센 고리와 A‑고리의 C1‑C3 디케톤·케톤‑엔올 토모르, C4의 디메틸아미노기가 항균 활성에 절대 필요함을 강조한다. C4‑S 입체배치는 그람‑음성균에 대한 효능을 좌우하고, C10‑페놀·C11‑C12 케톤‑엔올·12a‑OH는 리보솜 결합을 위한 보조 부위로 작용한다. 상부 말단(R1‑R3)과 하부 말단(R4‑R6)의 치환은 리포필리시티(logP)와 혈청단백질 결합률을 조절해 흡수·분포·대사 특성을 변형한다. 예를 들어, 미노사이클린의 0.5 logP는 높은 조직투과성을 부여해 신경보호 효과를, 티게사이클린의 0.8 logP는 광범위한 그람‑양·음성균에 대한 활성을 유지한다.
셋째, 비항균 활성을 설명하기 위해 저자는 ‘리포필리시티‑이온키레이트’ 메커니즘을 제시한다. TC는 Ca²⁺·Mg²⁺와 강하게 킬레이트하며, 이는 MMP 억제, 콜라게네이스 차단, ROS 생성 등 다양한 세포신호를 조절한다. 특히, CMT‑3(디메틸아미노 제거)와 같은 화학 변형체는 항염·항암 효과를 강화하면서 항균 활성을 크게 감소시킨다. 이는 ‘다중표적(chameleonic)’ 특성으로, 구조적 유연성(64가지 토모르·양성자화 형태)과 금속이온 결합이 복합적인 생물학적 결과를 만든다.
넷째, 저자는 1 325개의 TC 유도체를 PubChem 데이터베이스에서 90 % 유사도 기준으로 추출, 95 % 이상 고유성을 가진 112 종을 대상으로 ‘5원칙(rule of five)’과 물리화학적 파라미터를 정량화했다. 이를 통해 로그P, 용해도, 장내 흡수율, 혈청단백질 결합률, 신장 청소율, 반감기 등의 PK 데이터를 표 1에 정리하고, 각 파라미터가 구조 변형과 어떻게 연관되는지를 시각화하였다.
전체적으로 논문은 테트라사이클린을 단일 항균제에서 ‘다중표적 플랫폼’으로 재정의하고, 구조적 변형이 리포필리시티·금속이온 결합·톤머 전환을 통해 다양한 치료 영역(염증, 신경퇴행, 바이러스, 암)으로 확장될 수 있음을 설득력 있게 제시한다. 향후 신약 설계 시, C4 아미노기의 입체배치 유지와 동시에 D‑고리의 리포필리시티 조절, 금속이온 킬레이트 능력 강화가 핵심 전략이 될 것으로 전망된다.
**
댓글 및 학술 토론
Loading comments...
의견 남기기