단백질 접힘의 온도 안정성 및 속도에 미치는 제한 효과: Ising‑유사 모델을 통한 정량적 고찰
초록
Wako‑Saito‑Muñoz‑Eaton(WSME) 모델을 일반화하여 6가지 단백질(이상적인 α‑헬릭스·β‑시트와 실제 3‑헬릭스 번들·Protein G·그의 C‑말단 β‑헤어핀)을 두 평행벽 사이에 가두었다. 제한 거리 2R을 변화시키며 두 단계의 제한 구역을 확인했으며, 약한 제한에서는 접힌 상태가 안정화되고, 강한 제한에서는 열적 안정성 및 접힘 속도가 감소한다. 약한 제한 영역에서 전이 온도와 접힘 속도의 로그는 R⁻ᵞ 형태로 스케일링되며, γ는 1.42~2.35 사이로 추정된다.
상세 분석
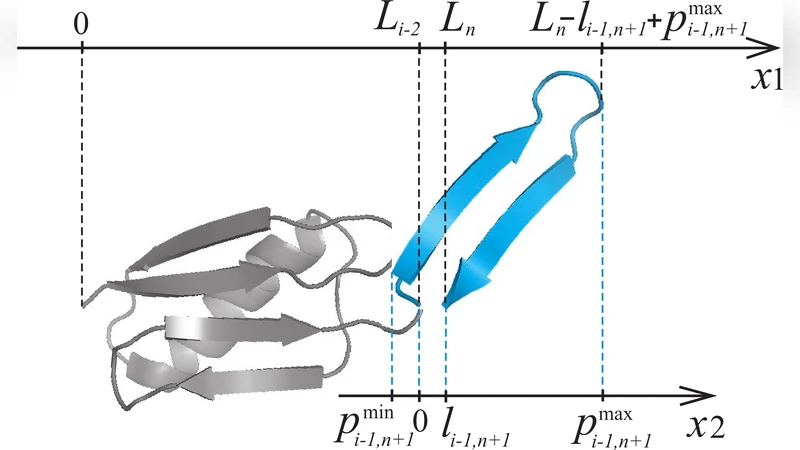
본 연구는 전통적인 WSME 모델에 공간적 제한을 도입한 확장형을 제안한다. 단백질을 N개의 이진 변수 mₖ(1: native, 0: unfolded)로 기술하고, 원자 간 접촉 에너지 εᵢⱼ와 접촉 행렬 Δᵢⱼ을 이용해 전체 해밀토니안을 구성한다. 제한을 구현하기 위해 각 원소가 두 벽 사이에 존재하도록 ‘최대 길이 p_maxᵢⱼ’와 ‘최소 길이 p_minᵢⱼ’를 계산하고, 재귀식(4,5)에 Heaviside 함수 θ를 삽입해 물리적으로 허용되는 구성을 필터링한다. 또한, 단순히 끝‑끝 거리 L이 아니라 ‘효과적 길이’(가장 먼 두 잔기의 거리)를 사용해 번역 자유도를 보정한다. 이는 제한된 공간 안에서 동일한 내부 구조를 갖는 구성들이 서로 다른 위치에 존재할 수 있음을 반영한다.
계산은 길이 해상도를 0.1 Å로 제한해 효율성을 확보했으며, 실제 단백질(1PRB, 2GB1)과 이상적인 구조(α‑헬릭스, 2‑strand β‑시트, 3‑strand β‑시트)를 대상으로 자유 에너지, 비열, 평균 native 잔기 비율 등을 2R을 변화시키며 평가했다. 결과는 두 개의 제한 구역을 명확히 보여준다. 첫 번째 구역(2R > L_N^eff)에서는 비‑native 풀의 확장된 구성들이 억제돼 엔트로피 감소가 일어나고, 접힌 상태가 상대적으로 안정화된다. 특히 3‑헬릭스 번들에서는 native와 non‑native 모두가 안정화되지만, native가 약간 더 큰 안정화 효과를 보인다. 반면, Protein G의 C‑말단 헤어핀은 native와 non‑native 모두가 불안정해지며, 비‑native가 더 크게 영향을 받아 전체 전이 온도가 낮아진다. 두 번째 구역(2R < L_N^eff)에서는 native 자체가 제한에 의해 억제되어 전이 온도가 급격히 감소한다.
동역학적 측면에서는 Monte‑Carlo 시뮬레이션을 이용해 접힘 속도 k_f를 측정했으며, log k_f와 전이 온도 ΔT_f가 R⁻ᵞ 형태로 스케일링됨을 확인했다. 추정된 γ 값은 1.42~2.35 사이로, 이론적 예측(γ = 2 for ideal Gaussian chain, γ = 5/3 for excluded‑volume chain 등)과 실험·시뮬레이션 결과 사이에 위치한다. 이는 제한이 단백질의 자유 에너지 지형을 복합적으로 변형시키며, 구조적 콤팩트성, 접촉 네트워크, 그리고 번역 자유도가 γ에 영향을 미친다는 점을 시사한다.
본 논문의 주요 공헌은 (1) WSME 모델에 공간적 제한을 정확히 포함하는 수학적 프레임워크를 제공, (2) 제한이 열역학적 안정성과 동역학적 속도에 미치는 비선형 효과를 정량화, (3) 다양한 구조에 대해 γ가 1.4~2.4 사이로 변동함을 보여줌으로써 기존 이론과 실험 사이의 격차를 메우는 데 기여했다는 점이다.
댓글 및 학술 토론
Loading comments...
의견 남기기