DNA 복제의 양자 얽힘 교환 모델
초록
본 논문은 DNA 복제 과정에서 핵산 염기의 인식과 상보적 결합을 양자 정보 이론으로 재해석한다. 저자는 염기 내부에서 전자·양성자 이동에 의해 발생하는 퀴노톤 얽힘(내부 얽힘)이 상보적인 염기와 결합할 때 얽힘 교환을 통해 서로 다른 염기 사이에 새로운 얽힘(외부 얽힘)이 형성된다고 제안한다. 이를 구현하기 위한 화학적 회로와 디코히런스 자유 서브스페이스(DFS) 활용 방안을 논의하고, 실험적 검증 가능성을 탐색한다.
상세 분석
이 논문은 전통적인 생화학적 설명이 분자 구조와 전자 배치를 통해 효소 작용을 기술하는 데 한계가 있음을 지적하고, 양자 정보 과학의 개념을 생물학적 시스템에 적용함으로써 새로운 메커니즘을 제시한다. 핵심 가정은 ‘염기 인식이 내부 얽힘을 유도한다’는 것으로, 이는 특정 염기가 효소(DNA 폴리머레이스)의 활성 부위에 결합하면서 해당 염기의 퓨리미딘·피리미딘 고리 내에서 서로 다른 툰머 형태(예: 케톤‑엔올 전이)가 양자 중첩 상태로 존재한다는 의미이다. 이러한 내부 얽힘은 전자·양성자 전이와 수소 결합 네트워크에 의해 빠르게 생성되며, 그 지속 시간은 주변 수용액의 열적·전기적 잡음에 의해 제한된다.
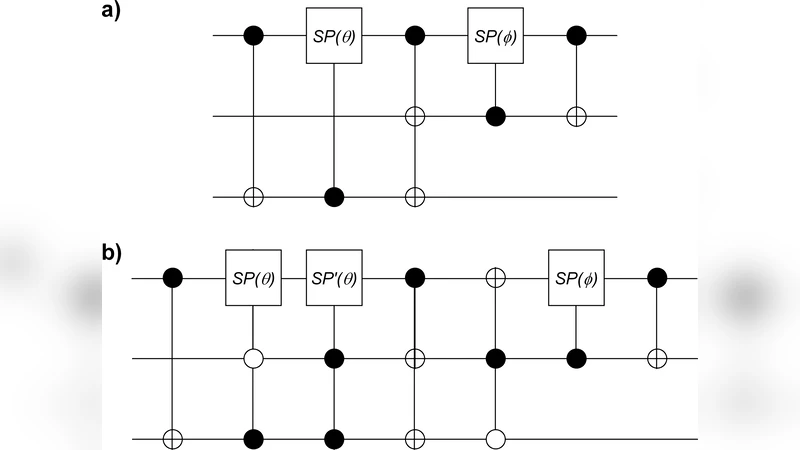
다음 단계는 상보적인 염기와의 결합 과정이다. 저자는 이 과정을 ‘얽힘 교환(entanglement swapping)’이라고 부른다. 구체적으로, 두 염기가 서로 맞닿아 수소 결합을 형성할 때, 각각의 내부 얽힘이 외부 얽힘으로 전이하면서 두 염기 사이에 새로운 양자 상관관계가 형성된다. 이는 양자 회로에서 CNOT·Hadamard 연산을 연속적으로 적용해 두 큐비트의 얽힘을 교환하는 프로토콜과 유사하다. 논문은 이러한 교환이 효소의 구조적 변형(예: 폴리머레이스의 ‘손가락’ 도메인 움직임)과 연계되어, 얽힘이 실제 화학 결합 에너지로 전환된다고 가정한다.
디코히런스 문제를 해결하기 위해 저자는 ‘디코히런스 자유 서브스페이스(DFS)’ 개념을 도입한다. 세포 내 물리적 환경은 고온·수용액 상태이지만, 특정 대칭성(예: 스핀-1/2 전자·양성자 쌍의 전체 스핀 보존) 하에서 시스템은 외부 잡음에 대해 불변인 서브스페이스에 머무를 수 있다. 따라서 내부 얽힘과 외부 얽힘 모두 이러한 DFS에 매핑되면, 열적 디코히런스가 억제되어 양자 정보가 충분히 오래 지속될 수 있다.
생화학적 구현 방안으로는 (i) 툰머 전이를 촉진하는 금속 이온(예: Mg²⁺)의 배위, (ii) 광학적 펄스(초단 파장 레이저)를 이용한 전자·양성자 전이 제어, (iii) 단백질 내 전자 전달 체인(예: 철‑황 클러스터) 활용을 제시한다. 각각은 양자 회로의 ‘게이트’에 해당하며, 효소-DNA 복합체 내부에서 순차적으로 작동한다는 가정이다.
마지막으로 논문은 실험 검증을 위해 (a) 핵자기공명(NMR)·단일분자 전자스핀공명(ESR)으로 툰머 중첩 상태 감지, (b) 초고속 라만 스펙트로스코피로 얽힘 교환 순간 포착, (c) 인공 DNA 복제 시스템에 양자 얽힘 억제제(디코히런스 촉진제)를 투입해 복제 효율 변화를 측정하는 전략을 제안한다. 전반적으로 이 연구는 양자 정보 이론을 생물학에 적용함으로써 기존의 ‘화학적 반응 경로’ 모델을 보완하고, DNA 복제의 정확성과 속도에 대한 새로운 물리적 설명을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기