양자 단백질학 전자구조와 전기쌍극자 모멘트 기반 새로운 연구 분야
초록
본 논문은 양자역학과 단백질체학을 결합한 ‘양자 단백질학’이라는 새로운 학문 영역을 제안한다. 선형 스케일 반응성 반응계산(MOZYME, PM6, COSMO)을 이용해 메탄균 Mth의 6개 단백질 전자구조와 전기쌍극자 모멘트를 계산하고, 전기쌍극자 크기를 단백질 특성화 지표로 활용한다는 아이디어를 제시한다.
상세 분석
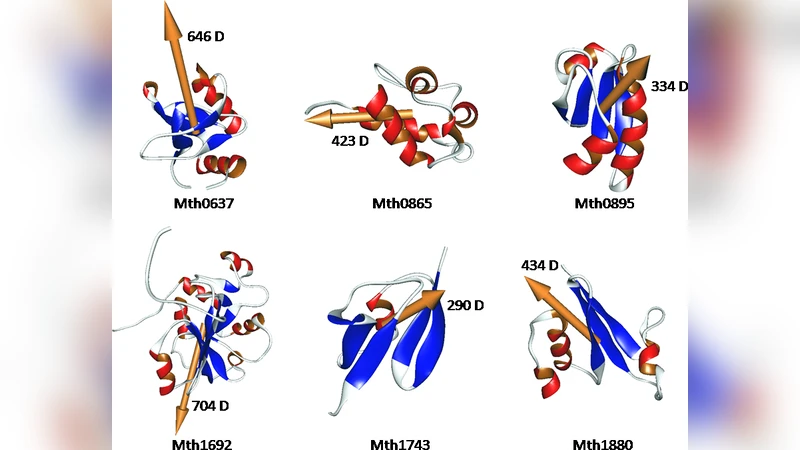
논문은 먼저 인간 게놈 프로젝트 이후 단백질체학이 급성장했지만, 3차원 구조만으로는 전자적 특성을 충분히 설명하기 어렵다는 점을 지적한다. 이를 보완하기 위해 저자는 선형‑스케일 양자화학 프로그램인 MOPAC2009의 MOZYME 알고리즘을 활용한다. MOZYME는 단백질의 루이스 구조를 초기 밀도 행렬로 사용해 지역화된 오비탈을 빠르게 수렴시키며, 반경 수천 원자까지도 실용적인 시간 안에 계산할 수 있다. 반응성 파라미터는 최신 반경‑반경 반응성 파라미터인 PM6를 적용하고, 용매 효과는 COSMO 모델(ε=78.4)로 포함한다. 이렇게 얻은 전자 에너지 레벨, 아미노산 측쇄 전하, 전기정전위, 그리고 영구 전기쌍극자 모멘트(μ)를 전자구조 지표로 제시한다. 특히 μ≠0 Debye라는 사실을 근거로, 모든 단백질은 고유한 전기쌍극자를 가지고 있으며, 이는 단백질 간 전자적 차이를 정량화하는 간단하면서도 직관적인 매개변수로 활용될 수 있다. 저자는 Mth의 6개 단백질(1JRM, 1IIO, 1ILO, 1JCU, 1RYJ, 1IQS)을 선택해 NMR 구조를 그대로 사용, 별도의 최적화 없이 전자구조를 계산하였다. 결과는 단백질 크기(N_A)와 채워진 궤도(N_L)가 전자쌍극자 크기에 영향을 미치며, 전하 상태(양전하, 중성, 음전하)와는 별개로 μ가 수백 Debye에 달함을 보여준다. 또한, 전하를 띤 단백질 주변의 반대 전하 이온이 μ의 방향과 크기에 큰 영향을 주지 않는다는 점을 이전 연구와 연계해 설명한다. 저자는 이러한 전기쌍극자 정보를 이용해 단백질을 전자구조 기반으로 분류하고, 향후 전자구조 데이터베이스와 MD 시뮬레이션을 결합해 기능적 해석을 확대할 수 있음을 제안한다. 그러나 반경‑반경 반응성 방법의 근사성, NMR 구조의 불확실성, 전기쌍극자 계산 시 기준점 선택(질량 중심 vs 전하 중심) 등 한계점도 명시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기