나노입자에 대한 대식세포 반응: 티타늄산화물 vs 구리 나노입자 프로테오믹스 분석
초록
본 연구는 골수 유래 마우스 대식세포에 티타늄산화물(TiO₂)과 구리(Cu) 나노입자를 24시간 처리한 뒤 2‑D 전기영동 기반 프로테오믹스 분석을 수행하였다. TiO₂는 대사 경로와 저산소 반응 단백질을, Cu는 산화 스트레스와 단백질 재배열을 주로 유도했으며, 두 나노입자는 서로 다른 단백질 변화를 보여 대식세포의 특이적 반응을 시사한다.
상세 분석
이 논문은 나노입자(NP)의 생물학적 위험성을 평가하기 위해, 환경에 널리 퍼진 TiO₂와 항균 특성을 가진 Cu 나노입자를 골수 유래 마우스 대식세포에 노출시킨 후 전반적인 단백질 발현 변화를 탐색한 연구이다. 실험 설계는 두 가지 주요 요소로 구성된다. 첫째, 대식세포는 7일 배양 후 CD11b⁺/CD14⁺ 표지자를 통해 성숙을 확인하고, LPS 자극에 대한 TNF‑α와 NO 분비능력을 검증함으로써 기능적 활성을 확보하였다. 둘째, NP는 0.2 % PVP40으로 코팅해 생물학적 매체에서의 응집을 최소화했으며, DLS 측정으로 배양 24 h 후 평균 입경이 TiO₂는 약 319 nm, Cu는 약 428 nm임을 확인하였다.
노출 농도는 각각 100 µg/mL(TiO₂)와 10 µg/mL(Cu)로, 세포 생존률이 80 % 이상 유지되는 LD₂₀ 수준을 선택하였다. 이는 급성 독성을 피하면서도 기전 수준의 변화를 포착하기 위한 전략이다. 단백질 추출은 고농도 요오드화 우레아/티오우레아 용액으로 이루어졌으며, 2‑D 전기영동(4–8 pH IEF, SDS‑PAGE) 후 은색 염색으로 시각화하였다. Delta2D 소프트웨어를 이용해 1.5‑배 이상 변화된 스팟을 선정하고, MALDI‑TOF/TOF MS/MS로 정체를 규명하였다.
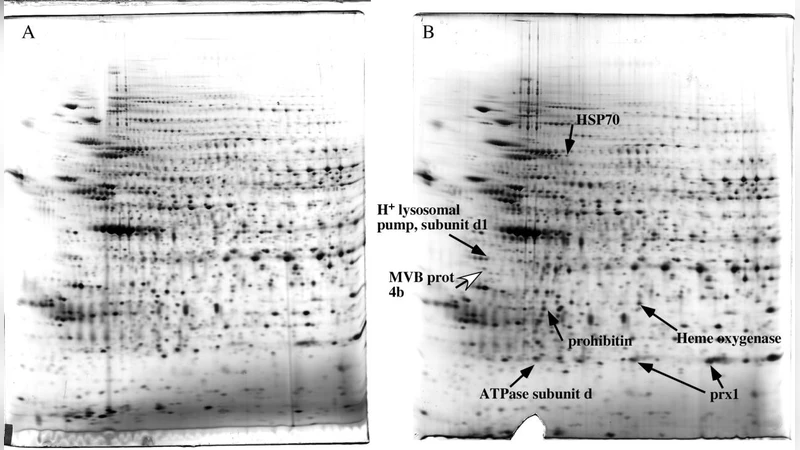
TiO₂ 처리에서는 대사 효소(말산 탈수소효소, 알데히드 탈수소효소, 글루코시다제)와 미토콘드리아 외부단백질(VDAC), 항산화 효소(Prx4), 프로테아좀 알파6 서브유닛, G‑단백질 베타1(Gnb1), 철 저장 단백질 페리틴, 저산소 반응 단백질(O₂‑regulated protein) 등이 상승하였다. 이는 전반적인 대사 촉진과 저산소 유사 환경을 유도함을 시사한다. 반면, Cu 처리에서는 ATPase subunit d, 프로히비틴, HSP70 등 스트레스 반응 단백질과 함께, 산화 스트레스 마커인 헴옥시다제와 산화된 형태의 Prx1이 4배 가량 증가하였다. 특히 Prx1의 산화형 증가는 심각한 ROS 손상을 의미한다. 또한, 다중소포체 단백질(MVB prot4b) 감소와 H⁺‑리소좀 펌프 d1 서브유닛 증가가 관찰돼, 엔도솜‑리소좀 경로의 재구성이 일어났음을 보여준다.
두 나노입자군 사이에는 겹치는 단백질이 없으며, TiO₂는 대사와 저산소 반응을, Cu는 강력한 산화 스트레스를 주도한다. 이는 금속 특성(비레독스성 TiO₂ vs 레독스성 Cu)이 대식세포 내 신호 전달 및 세포 내 소기관에 미치는 차이를 반영한다. 연구는 2‑D 기반 프로테오믹스가 나노입자 독성 메커니즘을 포괄적으로 파악하는 데 유용함을 입증했으며, 향후 정량적 LC‑MS/MS, 시간 경과에 따른 동역학 분석, 그리고 인간 대식세포 모델 적용을 통해 위험 평가의 정밀도를 높일 필요성을 제시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기