자기장으로 제어하는 나노복합 멤브레인, 맞춤형 약물 전달 플랫폼
초록
본 연구는 초자성 나노입자와 온도감응성 나노젤을 함유한 복합 멤브레인을 개발하여, 교류 자기장을 가하면 멤브레인의 투과성을 온·오프 전환시킴으로써 약물 방출을 정밀하게 조절한다. 나노젤의 상전이 온도, 로딩량, 멤브레인 두께를 설계 변수로 삼아 방출 속도를 수십 배까지 변조할 수 있으며, 500 Da에서 40 kDa까지 다양한 분자량의 약물을 동일한 장치로 전달한다.
상세 분석
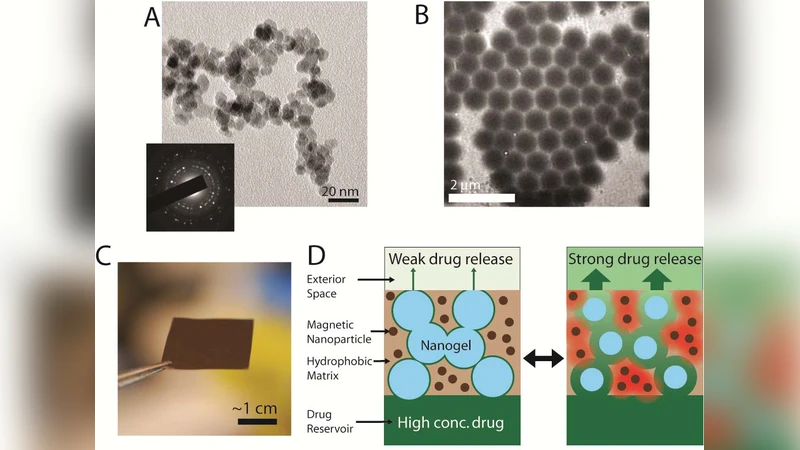
이 논문은 초자성 철산화물 나노입자와 PNIPAm 기반 온도감응성 나노젤(NG)을 에틸셀룰로스 매트릭스에 분산시켜 만든 복합 멤브레인의 설계·특성·응용을 체계적으로 분석한다. 나노젤의 상전이 온도는 NIPAm을 NIPMAm·AAm과 공중합함으로써 32 °C부터 46 °C까지 연속적으로 조절 가능했으며, 전이 온도 변화가 부피 수축 비율에 미치는 영향은 통계적으로 유의하지 않았다(p > 0.2). 자기장을 인가하면 초자성 나노입자가 고주파 교류에 의해 국부 가열·진동을 일으키고, 이 열에 의해 나노젤이 수축하면서 멤브레인 내부에 형성된 무질서한 기공 네트워크가 급격히 확대된다. 결과적으로 약물의 확산 저항이 감소해 ‘온’ 상태에서의 투과율이 크게 증가한다.
멤브레인 두께는 방출 속도에 직접적인 영향을 미치며, 90 µm(±14 µm)에서 288 µm(±32 µm)까지 두께를 늘릴 경우 방출량이 6.4 µg·h⁻¹에서 0.4 µg·h⁻¹로 1 order magnitude 감소한다(R² = 0.92). 나노젤 로딩은 12 wt %에서 32 wt %까지 변화시켰을 때, 방출 속도가 로그 선형적으로 증가했으며( R² > 0.94), 동시에 온/오프 비율은 감소한다. 예를 들어 12 wt % 로딩에서는 온/오프 비율이 15.2 ± 2.6이었으나, 32 wt %에서는 6.0 ± 0.5로 떨어졌다. 이는 고 로딩 시 기공이 과도하게 형성돼 ‘새는’ 상태가 되기 때문이다.
모든 조건에서 방출은 24 h 이상에 걸쳐 제로오더(Zero‑order) kinetics를 보였으며(R² > 0.98), 온 상태와 오프 상태 모두에서 일정한 속도로 약물이 흐른다. 따라서 전체 투여량은 자기장 인가 시간에 비례해 정밀하게 조절 가능하다. 약물 종류에 따라서는 40 kDa FITC‑덱스트린과 같은 고분자도 온/오프 전환이 가능했으며, 양이온성 bupivacaine과 같은 작은 분자도 동일 멤브레인으로 전달되었다.
재현성 측면에서, 동일 멤브레인에 대해 4회 연속 온‑오프 사이클을 수행했을 때 방출량의 변동이 통계적으로 유의하지 않았(p > 0.07). 장치 간 변동은 고 로딩(≥32 wt %)에서는 거의 없었지만, 저 로딩(≤25 wt %)에서는 혼합 과정의 미세 차이로 인해 약간의 차이가 나타났다. 자동화된 혼합이 이러한 변동을 최소화할 수 있다.
결론적으로, 나노젤 상전이 온도, 로딩량, 멤브레인 두께를 설계 변수로 삼아 약물 방출 속도와 온/오프 대비를 폭넓게 조절할 수 있는 플랫폼을 제시했으며, 이는 맞춤형 온·오프 약물 전달 시스템으로 임상 전이 가능성을 크게 높인다.
댓글 및 학술 토론
Loading comments...
의견 남기기