피코초 단백질 동역학의 기능적 상태 의존성
초록
본 연구는 테라헤르츠(THz) 유전율 측정을 이용해 리소자임과 사이토크롬 c의 온도 의존적 피코초 동역학을 조사하였다. 네이티브 단백질은 두 개의 활성화 에너지(E₁≈0.1 kJ·mol⁻¹, E₂≈10 kJ·mol⁻¹)를 보이는 이중 아레니우스 거동을 보였으며, E₂는 용매‑단백질 계면의 β‑이완과 연관된 동적 전이와 일치한다. 반면 E₁은 구조적 집단 운동에 기인하며, 변성(denaturation)이나 리간드 결합 시 사라지거나 크게 감소한다. 산화 상태 변화는 E₁에 영향을 주지 않는다. 결과는 THz 광학이 단백질 내부의 집단 운동을 탐지할 수 있음을 시사한다.
상세 분석
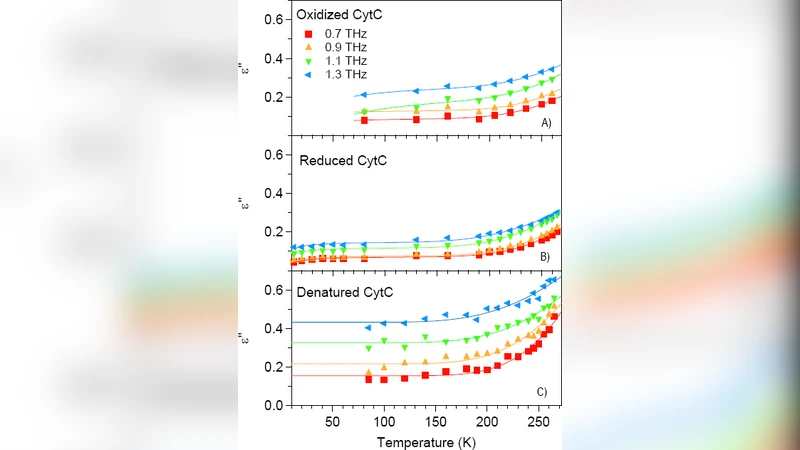
이 논문은 테라헤르츠 시간영역 분광법(TDS)을 이용해 수용액 내 단백질의 복소 유전율(특히 허수부 ε”)을 0.2–2.0 THz 범위와 100–300 K 온도 구간에서 측정함으로써 피코초 시간 스케일의 동역학을 정량화한다. 두 종류의 모델 단백질, 즉 129개의 아미노산으로 구성된 헨 에그 화이트 라이소자임(HEWL)과 105개의 아미노산을 가진 사이토크롬 c(Cyt c)를 선택했으며, 각각의 네이티브, 변성(6 M GdmCl), 리간드 결합(HEWL‑3NAG), 그리고 Cyt c의 산화·환원 상태를 비교하였다. 온도에 따른 ε”의 변화는 두 개의 아레니우스 항을 합한 형태로 잘 설명되었으며, 저에너지 항(E₁≈0.1 kJ·mol⁻¹)은 네이티브 단백질에서만 뚜렷하게 관찰되었다. 이 값은 이전에 X‑ray 비탄성 산란에서 보고된 집단 진동 모드의 에너지와 일치한다. 반면 고에너지 항(E₂≈10 kJ·mol⁻¹)은 변성·결합 여부와 무관하게 유지되며, 이는 단백질 표면과 인접한 물 분자의 β‑이완(동적 전이, DT)과 연관된 것으로 해석된다. 변성 시 ε”가 전반적으로 증가하는 현상은 노출된 표면적이 증가함에 따라 ‘생물학적 물’의 양이 늘어나기 때문이라고 설명한다. 리간드 결합에 의해 ε”가 감소하는 것은 리간드가 결합 부위를 메워 물과의 접촉면을 축소시키고, 동시에 저에너지 집단 운동이 억제되기 때문으로 추정한다. Cyt c의 경우 산화 상태가 바뀌어도 ε”와 활성화 에너지 분포에 큰 차이가 없으며, 이는 물의 동역학보다 단백질 고유의 구조적 모드가 주된 기여를 함을 의미한다. 전체적으로 이 연구는 THz 영역이 물과 단백질의 복합적인 전기적 응답을 구분하고, 특히 저에너지 집단 운동을 민감하게 탐지할 수 있음을 보여준다. 또한, 온도 의존적 아레니우스 분석이 단백질의 기능적 상태(네이티브·변성·리간드 결합)와 직접적인 연관성을 갖는 새로운 해석 틀을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기