경로 기반 생물학적 사전지식을 활용한 견고한 유전자 네트워크 추정 방법
** 본 논문은 차등 발현 유전자 선별을 limma와 Random Forest로 강화하고, 선정된 분자 서명을 KEGG·Reactome 등 경로 데이터베이스와 연계해 사전 정보를 구축한다. 이후 Gaussian Graphical Model을 기반으로 하는 SIMoNe 패키지를 이용해 사전 정보를 가중치로 반영한 네트워크를 추정한다. 유방암 치료 반응(완전 병리학적 반응 vs 비반응) 데이터를 사례로 들어, 두 조건 간 조절 네트워크 차이를 …
저자: Marine Jeanmougin, Mickael Guedj, Christophe Ambroise
**
본 논문은 유전자 발현 데이터로부터 유전자 조절 네트워크를 추정하는 과정에서 발생하는 ‘가능한 네트워크 공간의 방대함’과 ‘표본 수의 부족’이라는 두 가지 근본적인 문제를 해결하고자, 생물학적 사전 정보를 경로 분석을 통해 정량화하고 이를 네트워크 추정에 직접 반영하는 새로운 프레임워크를 제안한다. 전체 흐름은 크게 세 단계로 구성된다.
첫 번째 단계는 차등 발현 유전자를 선별하는 과정이다. 기존의 단순 t‑검정은 소표본 상황에서 분산 추정이 불안정하고, 외란에 민감하다는 한계가 있다. 저자들은 이를 보완하기 위해 limma 패키지를 이용해 베이지안 방식으로 분산을 ‘moderated’ 하여 전체 유전자 집합의 정보를 공유하도록 하였다. 이어서 Random Forest 알고리즘을 적용해 limma에서 도출된 p‑값 기반 후보 유전자들을 변수 중요도 순으로 재정렬한다. Random Forest는 부트스트랩 샘플링과 OOB 오류를 활용해 잡음 유전자를 효과적으로 걸러내며, 재정렬된 유전자 집합은 PCA 시각화에서 두 조건(예: 치료 반응군 vs 비반응군)의 구분이 크게 향상되는 것을 확인한다. 또한, STRING 데이터베이스를 활용해 고신뢰도(PPI 점수 ≥0.9) 상호작용 파트너를 추가함으로써 ‘분자 서명’에 기능적 연관성을 부여한다.
두 번째 단계는 경로 분석이다. 선정된 분자 서명을 기반으로 KEGG, Reactome, BioCarta 등 공개된 경로 데이터베이스와 교집합을 구하고, 하이퍼지오메트릭 검정을 통해 각 경로가 서명에 과잉 포함되는지를 평가한다. 다중 검정 보정(FDR) 후 유의한 경로를 사전 정보로 채택한다. 여기서 중요한 점은 경로가 단순히 ‘집합’이 아니라, 해당 경로에 속한 유전자 쌍이 실제 네트워크에서 연결될 가능성을 높이는 ‘구조적 제약’으로 전환된다는 것이다.
세 번째 단계는 네트워크 추정이다. 저자들은 Gaussian Graphical Model(GGM)을 기반으로 하는 SIMoNe 패키지를 사용한다. SIMoNe는 L1‑penalized 최대우도 추정에 ‘group‑lasso’와 유사한 구조적 패널티를 추가해, 같은 경로에 속한 유전자 쌍에 대해 에지 생성 비용을 낮춘다. 즉, 사전 정보가 높은 가중치로 반영되어, 데이터가 희소하거나 잡음이 많을 때도 생물학적으로 의미 있는 에지를 유지한다. 또한, 다중 조건(예: pCR vs non‑pCR)에서 동시에 여러 GGM을 추정하는 멀티‑태스크 프레임워크를 적용해, 조건 간 공통 구조와 차이점을 동시에 파악한다.
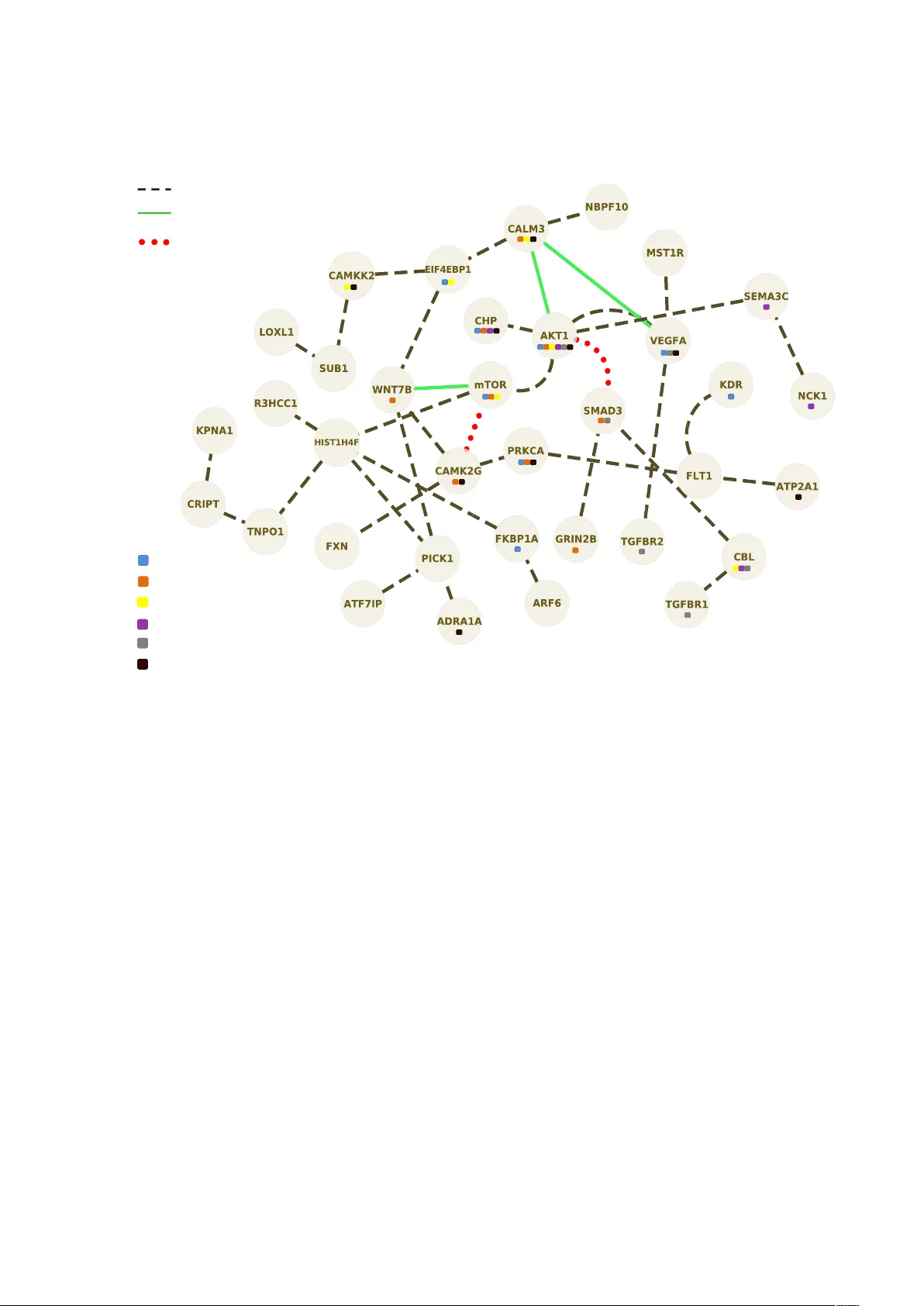
실험에서는 Hess et al. (2006) 유방암 데이터셋을 활용해, 병리학적 완전 반응(pCR)군과 비반응(non‑pCR)군의 네트워크를 각각 추정하였다. 두 네트워크를 비교한 결과, 세포주기, DNA 복구, PI3K/AKT 신호전달 등 기존 문헌에서 알려진 주요 경로가 양군 모두에서 핵심 모듈로 나타났으며, 특히 pCR군에서만 강하게 연결된 면역 관련 모듈과, non‑pCR군에서 강조된 스트레스 반응 모듈이 새롭게 도출되었다. 이러한 차별적 모듈은 치료 반응 메커니즘을 해석하는 데 직접적인 생물학적 통찰을 제공한다.
논문의 주요 기여는 다음과 같다. (1) 차등 발현 단계에서 limma와 Random Forest를 결합해 통계적 강건성을 확보하고, PPI 기반 기능 파트너를 추가함으로써 서명의 생물학적 일관성을 높였다. (2) 경로 분석을 통해 얻은 사전 정보를 GGM 추정에 구조적 패널티로 직접 반영함으로써, 데이터가 부족한 상황에서도 의미 있는 네트워크를 복원했다. (3) 멀티‑조건 GGM 추정을 통해 조건 간 네트워크 차이를 정량적으로 비교할 수 있는 통합 파이프라인을 제공했다.
한계점으로는 사전 정보가 기존 경로 데이터베이스에 크게 의존한다는 점이다. 최신 연구에서 밝혀진 새로운 경로나 아직 정의되지 않은 상호작용은 반영되지 않을 수 있다. 또한, GGM은 무방향 그래프를 제공하므로 인과 관계를 추정하려면 추가적인 모델링(예: 베이지안 네트워크, 동적 모델)이 필요하다. 향후 연구에서는 시간‑연속 데이터와 결합한 동적 GGM, 혹은 딥러닝 기반의 사전 학습 모델을 도입해 사전 정보를 보다 유연하게 업데이트하는 방안을 모색할 수 있다.
요약하면, 이 논문은 차등 발현 분석, 경로 기반 사전 구축, GGM 기반 네트워크 추정을 일관된 흐름으로 연결함으로써, 복잡한 유전체 데이터에서 신뢰할 수 있는 조절 네트워크를 도출하고, 임상적·생물학적 해석을 동시에 가능하게 하는 실용적인 방법론을 제시한다.
**
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기