종양 구형 모델링의 계산적 도전 과제
초록
본 논문은 대규모 종양 세포 집단과 구형체를 시뮬레이션하기 위한 계산적 접근법을 제시하고, 메모리·시간 복잡도 제한을 극복하기 위한 단계별 검증 전략을 논의한다. 세포 대사·세포주기 중심의 최소 모델을 구축하고, 폐쇄·개방 환경에서의 성장 및 치료 반응을 실험 데이터와 비교함으로써 모델의 신뢰성을 확보한다.
상세 분석
이 연구는 종양 구형체를 ‘중간 규모’ 실험 모델로 삼아, 전통적인 2D 배양과 실제 종양 사이의 격차를 메우려는 시도를 보인다. 저자들은 먼저 종양 성장의 다중 스케일 특성을 강조하고, 유전·비유전 요인(pH, 산소, 영양소, 세포외기질 등)이 미세환경에 미치는 영향을 정량화한다. 기존 모델이 임의 단위와 정성적 결과에 머무는 반면, 본 논문은 실제 실험값(세포 수, ATP 농도, 글루코스 섭취율 등)과 직접 매핑되는 파라미터를 도입한다.
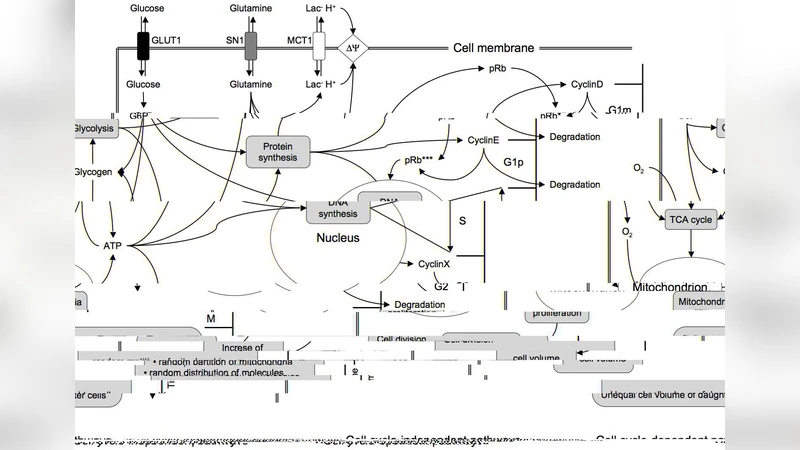
핵심은 ‘허브 기반’ 대사 네트워크 모델이다. 세포 내 수천 개의 반응을 모두 시뮬레이션하는 대신, 대사·신호망의 중심 허브(글루코스·글루타민 흡수, ATP 생산, 단백질·DNA 합성, 세포주기 조절 단백질인 pRb·사이클린)를 선택하고, 이들 사이의 흐름을 정량화한다. 이렇게 하면 메모리 요구량이 10^20 바이트 수준에서 10^9~10^10 바이트 수준으로 크게 감소한다. 또한, 세포 분열 시 미토콘드리아와 분자들의 무작위 분배, 다중 부위 인산화에 기반한 체크포인트 전이 등을 stochastic하게 구현해, 개별 세포 간 변동성을 재현한다.
계산 복잡도 측면에서 저자들은 O(N^2) 상호작용을 근사화하고, 시간 스텝을 세포 주기 수준(시간당 수십 분)으로 조정함으로써 시뮬레이션 속도를 실용적인 수준으로 끌어올렸다. 병렬화 전략으로 GPU와 멀티코어 CPU를 활용해 10^5~10^6 세포 규모의 구형체를 수일 내에 시뮬레이션한다.
실험 검증은 두 가지 환경(폐쇄형 배양 플라스크와 개방형 흐름 배양)에서 수행되었다. 폐쇄형에서는 영양소 고갈과 산성화가 성장 억제로 이어지는 것을, 개방형에서는 지속적인 영양 공급이 성장 속도를 유지시키는 것을 관찰했다. 모델은 이러한 차이를 ATP 생산량과 세포주기 길이 변화로 정확히 재현했으며, 항암제(예: 미토콘드리아 억제제) 투여 시 세포 사멸 비율과 사멸 위치(핵심부 vs 외부층)의 공간적 패턴도 실험과 일치했다.
결과적으로 이 논문은 ‘세포 수준의 미세환경·대사·신호’를 통합한 중간 복잡도 모델이, 완전 원자 수준 시뮬레이션이 불가능한 현재의 컴퓨팅 한계를 넘어, 실험과 정량적으로 연결될 수 있음을 증명한다. 이는 향후 개인 맞춤형 치료 시뮬레이션, 약물 스크리닝, 그리고 종양 성장 초기 단계의 역학 이해에 중요한 기반을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기