결합 메커니즘의 확장된 시각 유도 적합 구조 선택 독립 동적 구간
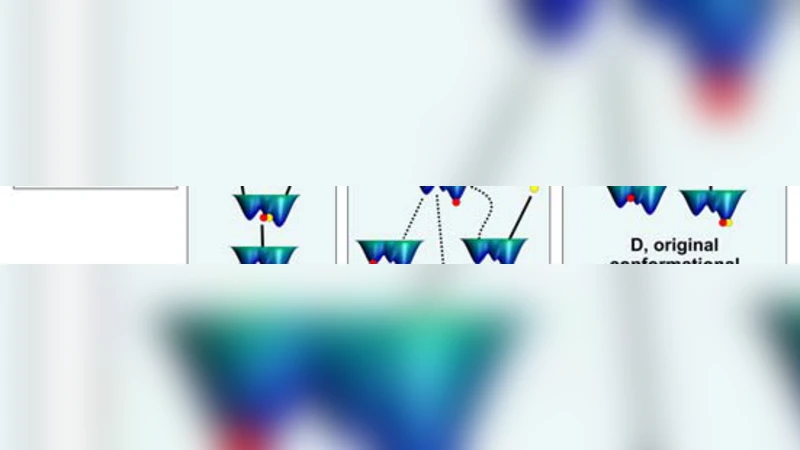
초록
단일분자와 NMR 연구가 드러낸 단백질 결합의 복잡성을 바탕으로, 저자들은 기존의 ‘구조 선택’ 모델을 확장하여 ‘유도 적합’까지 포괄하는 새로운 프레임워크를 제시한다. 특히, 전체 구조와 동적으로 구분되는 ‘이산 호흡기(디스크리트 브레이어)’라 불리는 독립적인 단백질 구간이 결합 과정에서 전이와 전구체 전환을 주도하며, 돌연변이에 민감하게 반응한다는 점을 강조한다. 또한, 이러한 동적 복합성은 단백질 응집, 신호 전달, 그리고 세포 내 혼잡 환경과도 깊은 연관이 있음을 논의한다.
상세 분석
본 논문은 단백질–리간드, 단백질–단백질 상호작용을 이해하는 데 있어 ‘구조 선택(Conformational Selection)’과 ‘유도 적합(Induced Fit)’이라는 두 전통적 메커니즘을 통합하는 확장 모델을 제안한다. 기존의 구조 선택 모델은 사전 존재하는 여러 미세구조 중에서 리간드가 가장 친화적인 형태를 ‘선택’한다는 가정을 기반으로 하지만, 실제 단백질은 결합 직후에도 국소적인 구조 재배열을 겪는다. 저자들은 이러한 재배열을 ‘조정(Adjustment)’ 과정으로 정의하고, 이는 유도 적합의 핵심 요소이지만 전체 메커니즘의 일부에 불과하다고 본다.
핵심적인 새로운 개념은 ‘독립 동적 구간(Independent Dynamic Segments)’ 혹은 ‘이산 호흡기(Discrete Breathers)’이다. 이 구간은 전체 단백질 매트릭스와는 다른 고유 진동 모드를 가지고 있으며, 에너지 집중 현상을 통해 국소적인 구조 변화를 촉진한다. 이러한 구간은 전이 상태의 에너지 장벽을 낮추고, 전구체(Pre‑transition)와 전이(Transition) 단계 사이의 커플링을 강화한다. 결과적으로, 이산 호흡기는 전이 경로를 선택적으로 ‘열어주어’ 결합 파트너에 대한 반응성을 조절한다.
돌연변이 분석 결과, 이산 호흡기가 위치한 잔기들은 일반적인 구조적 핵심 부위보다 변이 민감도가 높다. 이는 해당 구간이 에너지 흐름을 매개하고, 전이 상태의 안정성을 결정하기 때문에 작은 구조 변화에도 전체 결합 동역학에 큰 영향을 미친다는 것을 의미한다. 따라서, 질병 관련 변이의 대부분이 이산 호흡기 주변에 집중되는 현상을 설명할 수 있다.
또한, 저자들은 세포 내 ‘혼잡(crowding)’ 환경을 고려한다. 고농도 매크로분자들은 용매 효과와 부피 배제 효과를 통해 단백질의 자유 에너지 지형을 변형시킨다. 이러한 환경에서는 구조 선택과 유도 적합이 동시에 강화되며, 이산 호흡기의 역할이 더욱 두드러진다. 예를 들어, 혼잡한 환경에서 단백질이 부분적으로 ‘압축’되면, 이산 호흡기가 활성화되어 빠른 전이 경로를 제공하고, 이는 신호 전달 경로에서 빠른 응답성을 가능하게 한다.
마지막으로, 단백질 응집과 신호 전달 메커니즘에 대한 함의를 논의한다. 응집 초기 단계에서 부분적으로 노출된 이산 호흡기가 비특이적 상호작용을 촉진하여 올리고머 형성을 가속화한다. 반면, 신호 전달에서는 이산 호흡기가 특정 파트너와의 결합을 선택적으로 강화함으로써 ‘스위치’ 역할을 수행한다. 이러한 이중적 역할은 단백질이 동일한 동적 구조를 가지고도 상황에 따라 전혀 다른 기능을 수행할 수 있게 한다.
요약하면, 논문은 단백질 결합을 단순히 두 가지 메커니즘 중 하나로 보는 관점을 넘어, 선택‑조정‑전이의 연속적인 스펙트럼으로 재구성하고, 이 과정에서 독립 동적 구간이 핵심적인 ‘동적 촉매’ 역할을 한다는 새로운 통합 모델을 제시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기