단백질 항체의 물리적 특성이 혈류 내 이동 속도에 미치는 영향
초록
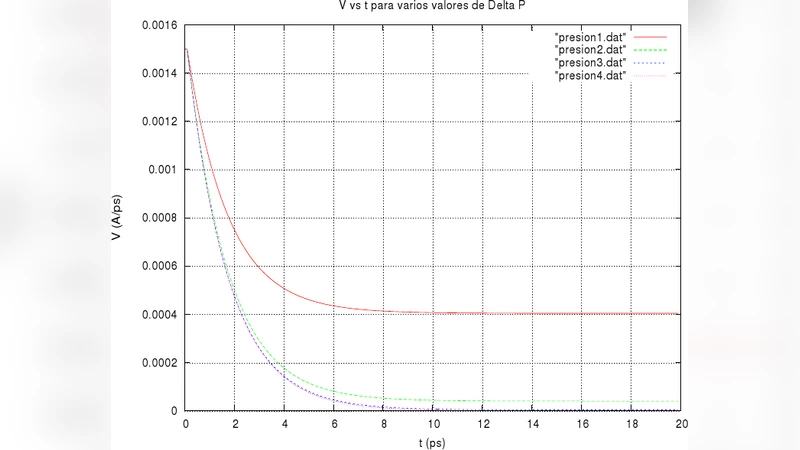
본 연구는 항체(모노클로날 항체)의 반경, 질량, 밀도와 혈관 내 압력 변화가 혈액의 층류와 포물선형 속도 분포 속에서 항체 이동 속도에 어떻게 영향을 미치는지를 수치적으로 분석한다. Verlet 알고리즘을 이용해 입자 운동 방정식을 풀었으며, 밀도를 고정했을 때 압력이 상승하면 항체 속도가 증가하고, 압력을 고정했을 때는 반경을 감소시키거나 밀도를 증가시킬 경우 속도가 상승한다는 결과를 제시한다.
상세 분석
이 논문은 항체와 같은 나노미터 규모 입자를 혈액이라는 복합 유체 내에서 모델링하려는 시도로, 물리학적 접근과 생물학적 응용을 연결한다는 점에서 의미가 크다. 저자는 먼저 혈관을 원통형 파이프로 가정하고, 흐름을 완전한 층류(parabolic laminar flow)로 설정했다. 이때 유체 속도는 r²에 비례하는 포물선형 분포를 따르며, Navier‑Stokes 방정식의 간소화 형태를 이용해 유도한다. 항체는 구형 입자로 가정하고, 질량 m, 반경 a, 밀도 ρₚ를 변수로 두었다. 입자에 작용하는 힘은 유체의 관성력, 점성 항력(Stokes drag), 그리고 압력 구배에 의한 구동력으로 구성된다.
수치해석에는 Verlet 알고리즘을 선택했는데, 이는 에너지 보존 특성이 뛰어나고 시간 단계가 작을 때 높은 정확도를 제공한다는 장점이 있다. 그러나 Verlet은 주로 보존계에 적합하고, 점성 손실이 큰 저레인즈 흐름에서는 오일러·맥클라클 같은 비보존형 스킴이 더 효율적일 수 있다. 또한, 논문에서는 시간 단계 Δt와 격자 해상도에 대한 수렴 검증이 부족하여 결과의 수치적 안정성을 판단하기 어렵다.
실험 변수 설정에서도 몇 가지 한계가 있다. 항체의 밀도를 고정하고 압력을 변화시켰을 때 속도가 증가한다는 결과는 압력 구배가 직접적인 구동력을 제공한다는 물리적 직관과 일치한다. 그러나 실제 혈관에서는 압력은 파동 형태로 변동하고, 혈관벽의 탄성도와 비뉴턴성 혈액 특성이 복합적으로 작용한다. 반경 감소가 속도 증가에 기여한다는 점은 Stokes drag ∝ a가 감소함을 의미하지만, 항체가 너무 작아지면 Brownian motion과 확산 효과가 무시할 수 없게 된다. 밀도 증가가 속도 상승을 초래한다는 결과는 관성력이 커져 유체 흐름에 더 잘 따라가게 된다는 해석이 가능하지만, 밀도 변화가 실제 항체 설계에서 구현 가능한 범위인지에 대한 논의가 부족하다.
결과 해석에서는 ‘kinetics’라는 용어를 속도 변화율로 정의했으나, 구체적인 수치(예: 평균 속도, 전이 시간)와 통계적 변동성을 제시하지 않아 재현성이 떨어진다. 또한, 혈류 속도와 압력 범위를 인간 대동맥 수준(≈ 100 mmHg, 0.3–0.5 m/s)으로 제한했는지 명시되지 않아, 실험적 적용 가능성을 판단하기 어렵다.
전반적으로 본 연구는 항체 물리적 파라미터와 혈류 역학 사이의 정량적 관계를 최초로 시도했지만, 모델 단순화, 수치 검증 부족, 생리학적 복합성 반영 미비 등의 한계가 있다. 향후 연구에서는 비뉴턴성 혈액 모델, 혈관벽 탄성, 그리고 항체‑표적 결합 동역학을 포함한 다중 물리 모델링을 도입하고, 실험적 마이크로플루이딕 검증을 병행한다면 보다 실용적인 설계 지침을 도출할 수 있을 것이다.
댓글 및 학술 토론
Loading comments...
의견 남기기