암세포를 죽이는 방법 컴퓨팅 모델이 밝힌 세포자멸사 인사이트
초록
암세포는 항아포토시스 단백질 과발현이나 프로아포토시스 인자 변이로 인해 사멸에 저항한다. 본 연구는 몬테카를로 시뮬레이션을 이용해 세포 간 변이와 공간적 이질성을 모델링하고, 실험적 검증을 통해 스트레스 강도와 경로 유형에 따라 사멸 속도가 달라짐을 확인했다. 특히, 단백질 양의 차이뿐 아니라 반응 자체의 내재적 확률적 변동이 일부 암세포의 생존을 초래한다는 새로운 메커니즘을 제시한다.
상세 분석
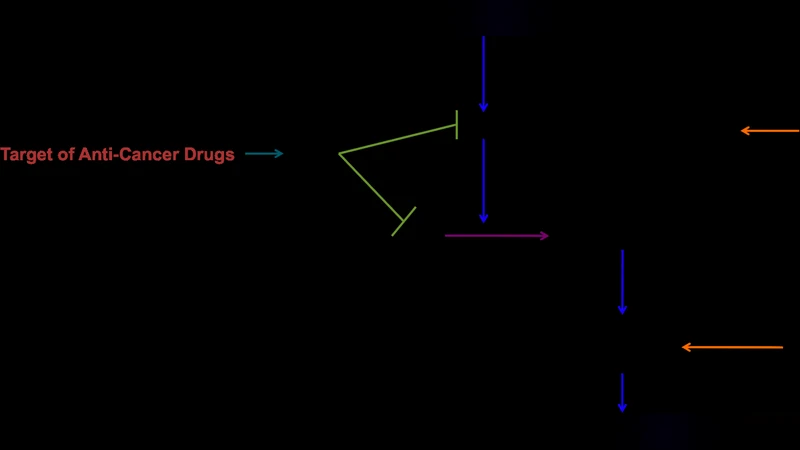
이 논문은 암세포가 항아포토시스 기전으로부터 회피하는 메커니즘을 정량적으로 규명하기 위해, 확률적 계산 모델인 몬테카를로 시뮬레이션을 핵심 도구로 활용하였다. 기존 연구에서는 주로 단백질 발현 수준의 변동이 사멸 효율에 미치는 영향을 다루었지만, 저자들은 세포 내 신호 전달 과정 자체가 본질적으로 확률적임을 강조한다. 이를 위해 먼저 주요 아포토시스 경로—내재성(미토콘드리아 매개)와 외재성(수용체 매개)—의 핵심 분자들을 정의하고, 각 반응 단계에 대한 전이 확률을 실험 데이터와 문헌값을 토대로 파라미터화하였다. 시뮬레이션은 개별 세포를 독립적인 에이전트로 취급해, 단백질 농도 분포, 공간적 확산 제한, 그리고 반응 시점의 무작위성을 동시에 고려한다.
시뮬레이션 결과는 두 가지 중요한 현상을 보여준다. 첫째, 스트레스 자극의 강도가 약할 경우, 세포군 전체에서 사멸 시작 시간이 넓은 분포를 보이며, 이는 “fractional killing”이라 불리는 현상의 근본 원인으로 작용한다. 둘째, 강한 자극 하에서는 대부분의 세포가 빠르게 사멸하지만, 여전히 소수의 세포가 내재된 확률적 변동 때문에 사멸을 회피한다. 특히, Bcl‑2와 같은 항아포토시스 단백질의 과발현이 있더라도, 시뮬레이션은 동일한 초기 조건에서도 사멸 여부가 무작위적으로 달라질 수 있음을 보여준다. 이는 기존의 “임계량” 개념을 보완해, 단순히 단백질 양만으로는 예측이 불가능한 ‘확률적 장벽’이 존재함을 시사한다.
또한, 저자들은 실험적 검증을 위해 동일한 암세포주에 대해 다양한 용량의 트라일레티노인 및 BH3 모방 펩타이드를 처리하고, 단일 세포 수준의 사멸 시간을 흐름세포계측(FACS)와 실시간 현미경으로 측정하였다. 실험 데이터는 시뮬레이션이 예측한 사멸 시간 분포와 높은 상관관계를 보였으며, 특히 저용량 처리 시 관찰된 ‘생존 세포의 꼬리’ 현상이 모델에 의해 재현되었다. 이는 모델이 실제 세포군의 이질성을 충분히 포착하고 있음을 뒷받침한다.
마지막으로, 논문은 이러한 확률적 모델링이 신약 개발 및 치료 전략에 미치는 함의를 논의한다. 기존의 ‘전체 세포 사멸률’만을 목표로 하는 약물 설계는, 실제 임상에서 관찰되는 부분적 사멸 현상을 충분히 설명하지 못한다. 확률적 변동을 고려한 모델은, 특정 단백질을 표적으로 하는 조합 요법이 ‘생존 꼬리’를 최소화하도록 최적화하는 데 활용될 수 있다. 예를 들어, Bcl‑2 억제제와 Mcl‑1 억제제를 동시에 투여하면, 각각의 확률적 저항 메커니즘을 동시에 차단함으로써 전체 사멸률을 크게 향상시킬 수 있다. 이러한 접근은 개인 맞춤형 치료 설계에도 적용 가능하며, 환자별 단백질 프로파일을 입력으로 하여 최적의 약물 조합과 용량을 예측하는 ‘인 실리코’ 플랫폼 구축의 초석이 된다.
요약하면, 이 연구는 암세포 사멸을 이해하는 데 있어 ‘양적 변동’뿐 아니라 ‘내재적 확률적 변동’까지 포괄하는 통합 모델의 필요성을 강조한다. 몬테카를로 기반 시뮬레이션은 실험적 관찰과 일치하는 사멸 시간 분포를 재현함으로써, 부분적 세포 사멸 현상의 메커니즘을 명확히 밝히고, 향후 치료 전략 설계에 실질적인 가이드를 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기