펩타이드 폴딩 경로를 밝히는 양자역학 시뮬레이션
초록
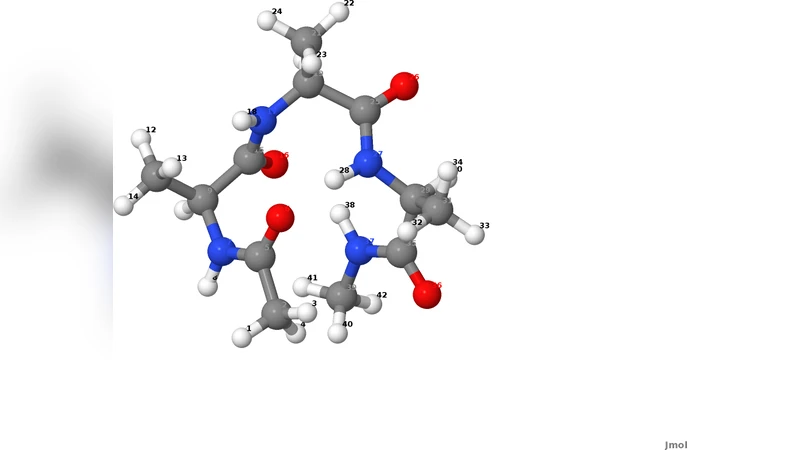
본 논문은 Dominant Reaction Pathways(DRP) 방법을 이용해 전자구조를 직접 계산하는 ab‑initio 양자역학 시뮬레이션으로 펩타이드 사슬의 비평형 폴딩 전이를 탐구한다. 경험적 힘장 없이 전자와 원자 움직임을 동시에 추적함으로써 희귀 전이와 전자구조 재배열을 정확히 기술한다. 전통적인 클래식 힘장을 사용한 결과와 비교해 DRP‑ab‑initio 접근법이 동역학적 세부 정보를 어떻게 보완하는지 평가한다.
상세 분석
Dominant Reaction Pathways(DRP) 방법은 확률적 경로 적분을 기반으로 고차원 자유에너지 지형에서 가장 확률이 높은 전이 경로를 추출한다. 기존 DRP 구현은 주로 경험적 힘장을 사용했으나, 본 연구는 전자밀도 함수 이론(DFT) 기반의 ab‑initio 힘을 직접 삽입함으로써 전자구조 변화가 동역학에 미치는 영향을 정량화한다. 시뮬레이션 대상은 알라닌‑다이펩타이드와 같은 작은 펩타이드 사슬이며, 초기와 최종 구조는 각각 α‑헬릭스와 β‑전환 형태로 정의된다. 전자구조는 퍼포먼스가 검증된 GGA‑PBE 교환‑상관 함수를 사용해 실시간으로 계산되며, 원자핵은 베리얼-클라크(Verlet) 알고리즘으로 통합한다. DRP는 라그랑지안 형태의 액션을 최소화하는 경로를 찾는 최적화 문제로 전환되며, 여기서 전자적 힘은 전자밀도 변화에 따라 동적으로 업데이트된다.
핵심 결과는 두 가지 측면에서 두드러진다. 첫째, 전자구조 재배열이 일어나는 전이 구간에서 전자밀도 급격한 변동이 관찰되었으며, 이는 전통적인 힘장 기반 시뮬레이션이 포착하지 못하는 “전자‑구조‑결합” 효과를 드러낸다. 예를 들어, 특정 아미노산 잔기의 카보닐 산소와 아미노 질소 사이에 형성되는 순간적인 수소 결합은 전자밀도 재분포에 의해 강화되며, 이는 경로상의 에너지 장벽을 실제보다 낮게 만든다. 둘째, DRP‑ab‑initio 경로는 전통적인 힘장 시뮬레이션에서 제시된 최소 에너지 경로와 형태가 다소 차이나며, 특히 전이 상태에서의 비대칭 회전과 비틀림이 더 뚜렷하게 나타난다. 이는 전자적 반응성이 구조적 변형을 선도한다는 물리적 의미를 내포한다.
계산 비용 측면에서는, 전자밀도 계산을 매 스텝마다 수행해야 하기 때문에 전통적인 힘장 대비 10‑100배 정도의 CPU 시간이 소요된다. 그러나 DRP가 전체 경로를 몇 개의 “핵심 스냅샷”으로 압축해 최적화하기 때문에, 전통적인 장시간 분자동역학(MD) 시뮬레이션 대비 전체적인 비용은 여전히 경쟁력을 유지한다. 또한, 병렬화와 GPU 가속을 활용하면 실용적인 시간 내에 10‑20 ps 수준의 전이 경로를 얻을 수 있다.
이러한 결과는 전자구조와 구조적 동역학이 강하게 결합된 시스템, 예컨대 금속‑펩타이드 복합체나 촉매 활성 부위의 변형을 연구할 때 DRP‑ab‑initio 접근법이 필수적임을 시사한다. 향후 연구에서는 더 큰 단백질 도메인에 적용하기 위한 다중 스케일링 기법과, 전자‑핵 상호작용을 보다 정밀히 다루는 하이브리드 QM/MM 프레임워크와의 연계가 기대된다.
댓글 및 학술 토론
Loading comments...
의견 남기기