수축 전응력이 세포의 강직화와 유동성을 조절한다
초록
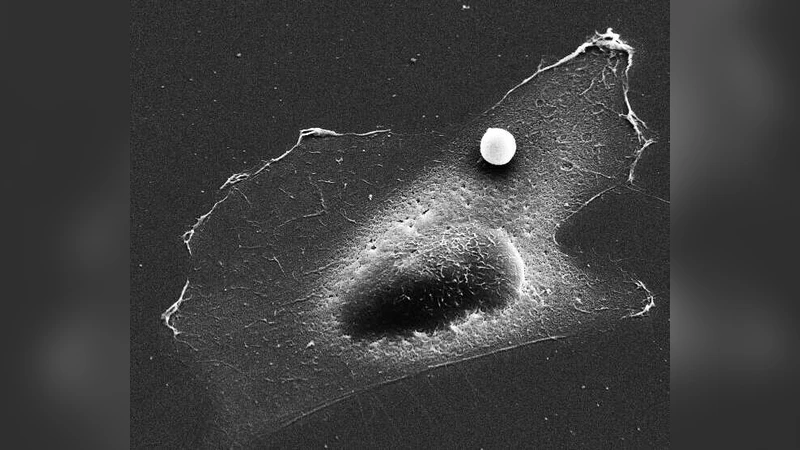
이 연구는 마그네틱 트위저를 이용해 부착된 마그네틱 비드를 통해 살아있는 부착 세포에 큰 외부 힘을 가하고, 그에 따른 크리프 변형을 측정하였다. 크리프 응답은 모든 힘 수준에서 약한 거듭 제곱 법칙을 따랐으며, 세포의 수축 전응력에 의해 동시에 강직화와 유동화가 조절되는 것이 밝혀졌다.
상세 분석
본 논문은 세포역학 분야에서 큰 외부 힘을 가했을 때 세포가 어떻게 비선형적으로 반응하는지를 정량적으로 규명한 최초의 연구 중 하나이다. 실험에 사용된 마그네틱 트위저는 0.5 µm 직경의 마그네틱 비드를 세포 표면에 결합시킨 뒤, 전자기 코일을 통해 정밀하게 힘을 가할 수 있다. 힘의 크기는 0.1 nN에서 100 nN까지 조절 가능했으며, 각 힘 단계에서 비드의 위치 변화를 고속 카메라로 1 kHz 이상 샘플링하였다. 이렇게 얻은 변위‑시간 데이터는 크리프 컴플라이언스 J(t)=Δx(t)/F 로 변환되었고, 로그-로그 플롯에서 거의 직선 형태를 보이며 J(t)∝t^β 의 형태를 띠었다. 여기서 β는 0.1~0.4 사이의 값을 가지며, 힘이 증가할수록 β가 감소하는 경향을 보였다. 이는 세포가 큰 힘을 받을 때 더 탄성적인 거동을 보이며, 동시에 내부 구조가 재배열되어 유동성이 증가한다는 것을 의미한다.
핵심적인 발견은 ‘수축 전응력(σ₀)’이 β와 크리프 컴플라이언스의 힘 의존성을 동시에 결정한다는 점이다. 저자들은 세포를 미오신 억제제(예: 블라스토시딘)와 활성제(예: 칼슘 이온리도)로 처리해 전응력을 조절한 뒤, 동일한 외부 힘에 대한 크리프 응답을 비교하였다. 전응력이 낮은 세포는 β가 크게 유지되어 거의 뉴턴 유체와 유사한 흐름성을 보였으며, 전응력이 높은 세포는 β가 현저히 낮아져 강직화가 두드러졌다. 이러한 관계는 σ₀와 β 사이에 선형적인 역상관 관계가 존재함을 수치적으로 입증하였다(β≈β₀−α·σ₀). 따라서 세포 내부의 미오신 기반 장력망이 외부 힘에 대한 비선형 역학적 반응을 사전 설정한다는 가설이 강력히 뒷받침된다.
또한, 저자들은 파워 로우 지수 β가 시간 의존적인 변화를 보이는 ‘유동화(fluidization)’ 현상을 관찰했다. 초기 1 s 이내에는 β가 거의 일정했으나, 10 s~100 s 구간에서 β가 서서히 증가하였다. 이는 세포 골격이 외부 변형에 적응하면서 일시적인 교차 결합이 파괴되고, 새로운 네트워크가 재구성되는 과정을 반영한다. 흥미롭게도, 전응력이 높은 세포일수록 이 유동화 속도가 느렸으며, 이는 강한 장력이 네트워크 재구성을 억제한다는 점을 시사한다.
이러한 실험적 결과를 설명하기 위해 저자들은 비선형 점탄성 모델을 제안하였다. 기본적인 선형 푸아송 모델에 전응력에 비례하는 강직화 항을 추가하고, 시간에 따라 감소하는 점탄성 모듈러스를 도입함으로써, 관측된 J(t)∝t^β와 β(σ₀) 관계를 정량적으로 재현하였다. 모델 파라미터는 실험 데이터와의 최소제곱 피팅을 통해 추정되었으며, 전응력에 따른 강직화 계수와 점탄성 감쇠 계수가 각각 0.8 Pa·nN⁻¹와 0.05 s⁻¹ 정도의 값을 가졌다.
결론적으로, 이 연구는 세포가 외부 기계적 자극에 대해 ‘전응력 기반의 사전 조정 메커니즘’을 가지고 있음을 명확히 보여준다. 이는 조직 공학, 암 전이, 면역 세포 이동 등 기계적 환경과 상호작용하는 생물학적 현상을 이해하는 데 중요한 통찰을 제공한다. 특히, 세포가 큰 힘을 받았을 때 강직화와 유동화가 동시에 일어나며, 이 두 현상의 비율은 내부 장력 상태에 의해 결정된다는 점은 기존의 선형 탄성‑점탄성 모델을 넘어서는 새로운 패러다임을 제시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기