상피 세포 확산의 화학·기계 신호 통합 모델
초록
본 연구는 상피 조직이 손상이나 외부 자극에 의해 확산할 때 나타나는 장거리 협동 현상을 설명하기 위해 최소한의 수학적 모델을 제시한다. 화학적 신호(예: 성장인자, 케이스톤)와 기계적 스트레스가 서로 영향을 주고받는 ‘케모-메카니컬’ 상호작용을 핵심으로 하며, 스트레스가 효소 활성도를 조절하고, 효소 농도가 세포의 수축력(traction)을 농도 의존적으로 변화시킨다. 모델 시뮬레이션은 실험에서 보고된 두 종류의 활성 파동—빠른 초기 파동과 느린 지속 파동—을 재현하고, 손상 부위와 자유 경계 조건에서 나타나는 전형적인 동역학 패턴을 구분한다. 결과는 화학·기계 신호가 각각 혹은 동시에 작용할 때 상피 확산이 어떻게 조절되는지를 정량적으로 설명한다.
상세 분석
이 논문은 상피 세포군이 손상 혹은 외부 기계적 풀림에 반응하여 집단적으로 이동하고 형태를 재구성하는 현상을, 기존의 단일 신호 모델이 설명하기 어려운 장거리 동기화 현상으로 규정한다. 저자들은 ‘케모-메카니컬’ 피드백 루프를 도입하여, (1) 기계적 응력 σ가 세포 내 신호전달 경로, 특히 MAPK 계열의 kinase 활성도를 촉진한다는 ‘스트레스‑케이스톤’ 효과와, (2) 활성된 kinase 농도 c가 세포가 기판에 가하는 traction force T를 비선형적으로 조절한다는 ‘농도‑트랙션’ 의존성을 수식화한다. 수학적으로는 연속체 역학 방정식과 반응‑확산 방정식을 결합한 편미분 방정식 체계를 구축했으며, σ와 c 사이의 상호작용을 선형 결합이 아닌, σ·c 형태의 곱셈항으로 표현해 비선형 증폭 효과를 강조한다.
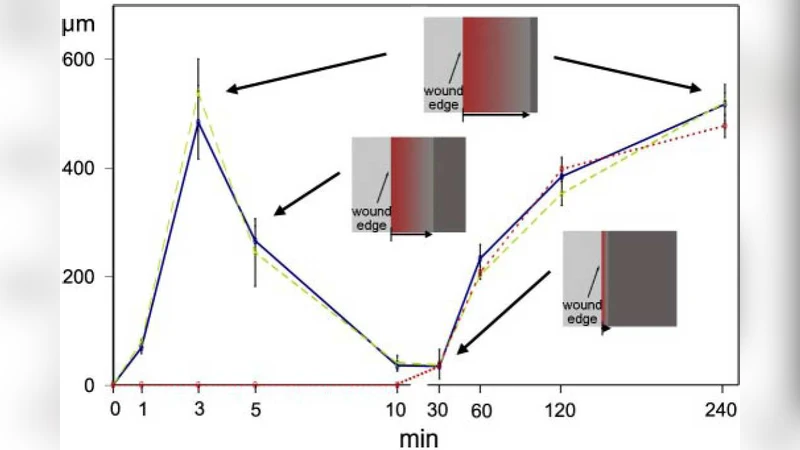
시뮬레이션 결과는 두 가지 시간 스케일의 파동을 생성한다. 첫 번째는 손상 직후 발생하는 급격한 σ 상승에 의해 즉시 촉발되는 ‘초기 파동’으로, 전파 속도가 실험값(≈10 µm·min⁻¹)과 일치한다. 두 번째는 초기 파동이 소멸한 뒤, c의 확산과 피드백에 의해 서서히 전파되는 ‘지속 파동’으로, 속도가 약 1 µm·min⁻¹ 수준이다. 이 두 파동은 각각 화학적 신호와 기계적 신호가 주도하는 메커니즘을 반영한다는 점에서, 모델이 실제 조직에서 관찰되는 복합적 동역학을 성공적으로 포착함을 보여준다.
또한 경계 조건을 바꾸어 ‘injury’(고정된 경계)와 ‘unconstraining’(자유 경계) 상황을 비교했을 때, 전자는 초기 파동이 강하게 억제되고 지속 파동이 주도적인 반면, 후자는 초기 파동이 크게 확대되고 전체 영역에 걸쳐 파동이 동시다발적으로 발생한다는 차이를 보였다. 이는 기계적 제약이 신호 전파 경로와 강도를 어떻게 조절하는지를 정량적으로 설명한다.
모델의 파라미터 민감도 분석에서는 스트레스‑케이스톤 계수와 농도‑트랙션 비선형 지수가 전체 동역학에 가장 큰 영향을 미치는 것으로 나타났다. 특히, 트랙션이 c에 대해 포화 형태(맥스웰‑볼츠만식)로 제한될 경우, 파동 전파가 급격히 감쇠하고 조직 재형성 속도가 감소한다. 이는 실제 세포가 과도한 수축력을 억제하기 위해 내부 피드백 메커니즘을 갖고 있음을 시사한다.
전체적으로 이 연구는 화학·기계 신호가 서로 얽혀 상피 조직의 장거리 협동을 이끌어내는 메커니즘을 최소 모델로 구현함으로써, 기존 실험 결과를 이론적으로 통합하고, 향후 조직 공학이나 상처 치유 전략에서 신호 조절을 설계하는 데 유용한 프레임워크를 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기