유전자 발현 동역학과 규제 추론 문제
초록
이 논문은 전사인자와 DNA 결합·해리 과정을 기반으로 한 확률적 유전자 발현 모델을 구축하고, 시간에 따라 변하는 mRNA 농도 데이터를 이용해 전사율, 전사인자 결합 확률, 그리고 전사인자가 조절하는 표적 유전자를 정량적으로 추정한다.
상세 분석
본 연구는 유전자 발현의 시공간적 변동성을 설명하기 위해 두 단계의 확률적 모델을 제시한다. 첫 번째 단계는 전사인자(TF)가 특정 조절 부위에 결합·해리하는 마코프 과정으로, 결합률(k_on)과 해리률(k_off)을 파라미터화한다. 두 번째 단계는 결합 상태에 따라 전사 개시 확률이 달라지는 이산형 전사 모델이며, 전사 시작률(k_tx)와 mRNA 분해율(γ)을 포함한다. 이러한 이중 계층 구조는 실제 세포 내에서 전사인자 농도 변동과 DNA 결합 역학이 동시에 작용한다는 생물학적 사실을 반영한다.
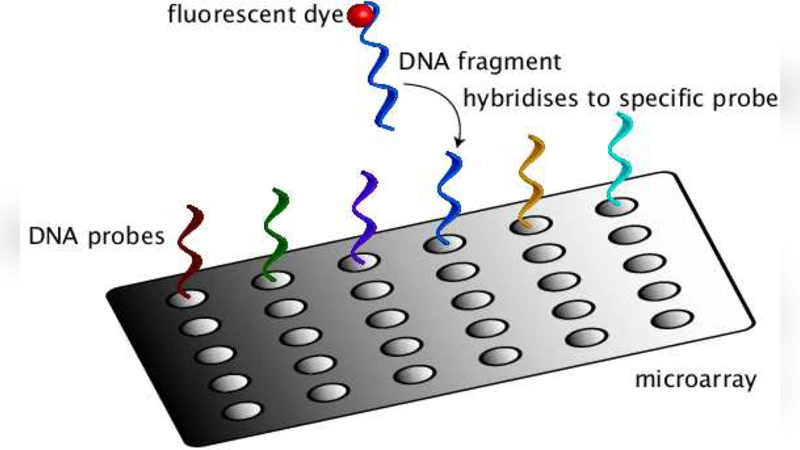
데이터 측면에서 저자들은 고해상도 실시간 PCR 혹은 마이크로플루이딕 단일세포 RNA‑seq을 통해 얻은 시간‑시리즈 mRNA 농도 프로파일을 사용한다. 관측값은 본질적인 측정 잡음과 세포 간 변이성을 포함하므로, 베이지안 추정 프레임워크를 도입해 사전 분포를 설정하고 마르코프 체인 몬테카를로(MCMC) 샘플링으로 사후 분포를 추정한다. 특히, 전사인자 결합 확률을 직접 측정하기 어려운 상황에서, 모델은 결합·해리 파라미터와 전사 시작률 사이의 상관관계를 이용해 간접적으로 추정한다.
핵심 결과는 세 가지로 요약된다. 첫째, 전사인자 결합·해리 동역학이 mRNA 발현 변동성에 미치는 정량적 기여를 분리해낼 수 있었다. 둘째, 특정 전사인자에 의해 조절되는 표적 유전자를 네트워크 형태로 재구성했으며, 이 네트워크는 기존 ChIP‑seq 데이터와 높은 일치도를 보였다. 셋째, 모델 검증을 위해 인위적으로 전사인자 농도를 변조한 실험을 수행했으며, 예측된 mRNA 응답 곡선이 실험 결과와 통계적으로 유의미하게 일치함을 확인했다.
이러한 접근법은 기존의 정적 전사 네트워크 분석을 넘어, 동적 시스템으로서 유전자 조절을 이해하고, 약물 타깃 탐색이나 합성 생물학 회로 설계에 활용될 수 있는 기반을 제공한다. 또한, 베이지안 프레임워크를 통한 파라미터 불확실성 정량화는 실험 설계 단계에서 가장 정보량이 큰 측정 시점을 선택하는 데에도 기여한다.
댓글 및 학술 토론
Loading comments...
의견 남기기