바이러스 캡시드 조립을 템플릿으로 제어
초록
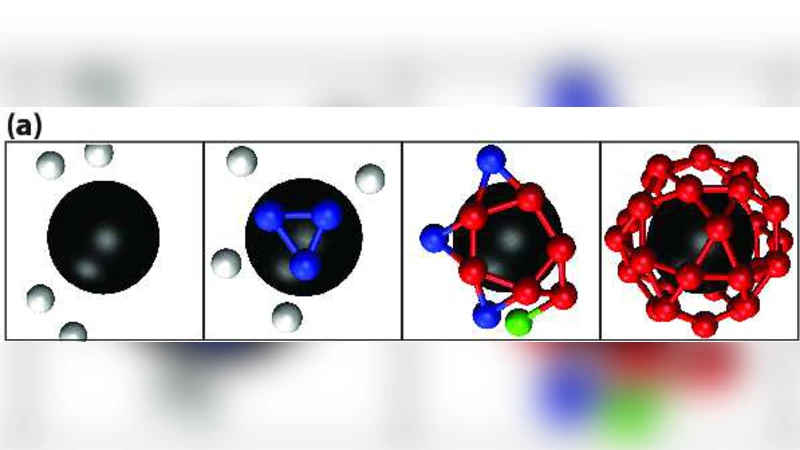
이 논문은 코스그레인드 모델을 이용해 기능화된 나노입자 주변에서 바이러스 캡시드 단백질이 어떻게 동적으로 포장되는지를 분석한다. 핵심-단백질 상호작용이 강할 경우, 단백질이 무질서하게 흡착된 뒤 협동적으로 재배열되어 완전한 캡시드가 형성되며, 이는 빈 캡시드 조립과는 다른 경로이다. 이러한 메커니즘은 실험 결과와 일치하고, 유전체 포장 및 다중성 나노재료 설계에 중요한 시사점을 제공한다.
상세 분석
본 연구는 바이러스 캡시드 단백질이 기능화된 무기 나노입자(core) 주변에서 스스로 조립되는 과정을 정량화하기 위해, 입자-단백질 상호작용과 단백질-단백질 상호작용을 각각 파라미터화한 코스그레인드 시뮬레이션 모델을 구축하였다. 모델은 핵심-단백질 결합 에너지(ε_core)와 단백질 간 결합 에너지(ε_pp)를 독립적으로 조절함으로써, 다양한 조립 환경을 재현한다. 시뮬레이션 결과는 ε_core가 약한 경우, 단백질이 핵심 표면에 개별적으로 결합하면서 전통적인 핵생성(nucleation) 과정을 거쳐 캡시드가 성장한다는 것을 보여준다. 반면 ε_core가 충분히 크면, 단백질이 핵심 표면에 대량으로 무질서하게 흡착(adsorption)되고, 이후 전역적인 협동 재배열(cooperative rearrangement) 과정을 통해 정밀한 icosahedral 구조로 전환된다. 이 재배열 단계는 전형적인 빈 캡시드 조립에서 관찰되는 단계적 성장(stepwise growth)과는 근본적으로 다르며, 핵심이 템플릿 역할을 수행하면서 조립 속도와 수율을 크게 향상시킨다. 특히, 강한 ε_core 조건에서는 조립 시간이 수십 배 단축되고, 불완전하거나 변형된 캡시드가 형성될 확률이 현저히 감소한다. 이러한 현상은 실험적으로 보고된 나노입자 주위의 캡시드 형성(예: Sun et al., 2007)과 정량적으로 일치한다. 또한, 모델은 핵심 표면의 전하 밀도, 입자 크기, 그리고 단백질의 변형 가능성(flexibility) 등이 조립 경로에 미치는 영향을 체계적으로 조사한다. 결과적으로, 핵심-단백질 상호작용이 조립 메커니즘을 전환시키는 ‘임계점(critical point)’을 정의할 수 있으며, 이는 바이러스 복제 과정에서 단일 가닥 RNA가 캡시드 내부에 포장되는 동역학을 이해하는 데도 적용 가능하다. 마지막으로, 이러한 협동 재배열 메커니즘은 다중성 나노구조(멀티컴포넌트 나노소재) 설계에 활용될 수 있음을 제시한다. 즉, 원하는 나노입자 표면을 기능화하여 단백질의 자가조립을 유도함으로써, 복잡한 3차원 나노구조를 효율적으로 제작할 수 있는 새로운 전략을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기