단일 분자 구조 변동의 증폭 및 검출 이중 피크 분포 단백질 네트워크 활용
초록
**
단일 효소의 구조 변동이 느린 경우, 제로차 초감도 인산화‑탈인산화 회로에 연결하면 변동이 수십 배 증폭되어 기질 인산화 수준이 이중 피크(바이모달) 분포를 보인다. 이를 통해 세포 내에서 효소의 구조 전이 속도를 비침습적으로 측정할 수 있다.
**
상세 분석
**
본 논문은 단일 효소가 여러 구조 상태 사이를 전이하면서 나타내는 동적 불균일성(다이나믹 디스오더)을, 전통적인 단일 분자 형광·전기화학 측정의 한계를 넘어 세포 수준에서 감지할 수 있는 방법으로 전환한다. 핵심 아이디어는 효소의 촉매 속도(k_cat)가 구조 전이 속도(k_conf)보다 빠를 때, 효소가 특정 구조에 머무는 시간 동안 생성되는 제품(또는 기질)의 농도가 급격히 변한다는 점이다. 이를 증폭시키기 위해 저자들은 ‘제로차 초감도 인산화‑탈인산화 사이클(Zero‑order ultrasensitive cycle)’이라는 작은 단백질 상호작용 네트워크를 도입한다. 이 회로는 두 효소(인산화 효소와 탈인산화 효소)가 각각 기질 S와 인산화된 기질 S∗를 상호 전환시키며, 반응 속도가 포화 상태에 도달하면 전체 시스템은 ‘초감도’ 특성을 보여 작은 입력 변화에도 큰 출력 변화를 만든다.
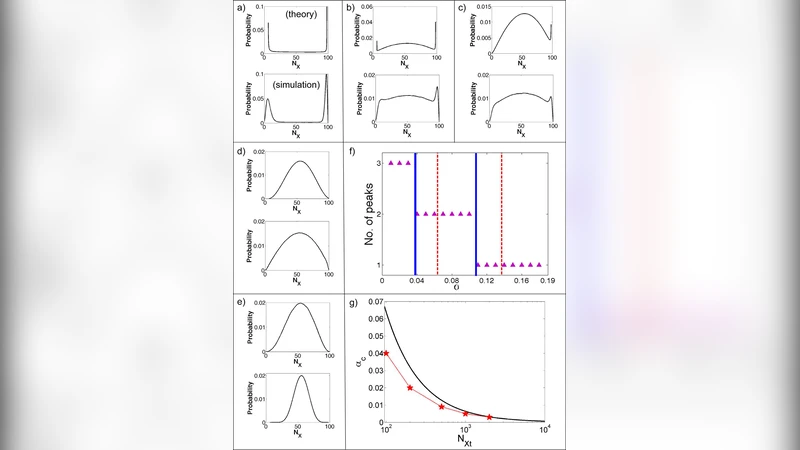
수학적으로는 마르코프 연속시간 체인을 이용해 효소의 두 구조 상태(E₁, E₂)와 각각의 촉매 상수(k₁, k₂)를 모델링하고, 전체 네트워크는 질량보존식과 Michaelis‑Menten 형태의 비선형 미분방정식으로 기술된다. 효소 전이가 느릴 경우(τ_conf ≫ 1/k_cat) 시스템은 장시간 동안 하나의 효소 상태에 고정되어 있어, S∗의 농도는 해당 상태에 대응하는 고정점 근처에 머무른다. 전이가 일어나면 급격히 다른 고정점으로 전이하면서 S∗ 농도가 크게 변한다. 이러한 ‘스위치‑같은’ 전이는 확률적으로 발생하므로, 장시간 관측 시 S∗ 농도 분포는 두 개의 뚜렷한 피크(바이모달)를 형성한다.
시뮬레이션 결과는 다음과 같다. (1) 효소 전이 속도가 촉매 속도보다 10배 이상 느릴 때 바이모달 분포가 명확히 나타난다. (2) 전이 속도가 촉매 속도와 비슷하거나 빠르면 분포는 단일 피크(정규분포)에 가까워진다. (3) 네트워크의 초감도 파라미터(예: 인산화 효소와 탈인산화 효소의 총 농도 비율)를 조절하면 증폭 정도를 수십 배에서 수백 배까지 조절 가능하다.
실험적 구현 방안으로는 (i) 인산화‑탈인산화 사이클을 재구성한 합성 생물학 회로, (ii) FRET 기반 인산화 센서를 이용한 실시간 S∗ 농도 측정, (iii) 단일 효소를 유전적으로 변형해 전이 속도를 조절하는 방법을 제시한다. 이러한 접근은 기존 단일 분자 형광 트레이싱이 요구하는 고가 장비와 복잡한 데이터 해석을 대체할 수 있으며, 세포 내에서 효소의 구조 전이 동역학을 ‘보고’ 동시에 기능적 결과(인산화 수준)를 동시에 기록할 수 있다.
이 연구는 동적 불균일성의 생물학적 의미를 재조명한다. 효소의 구조 변동이 세포 신호 전달, 대사 조절, 그리고 질병 상태(예: 암세포의 변이 효소)에서 어떻게 증폭되어 전체 네트워크에 영향을 미치는지를 정량적으로 분석할 수 있는 새로운 도구를 제공한다. 또한, 바이모달 분포 자체가 ‘디지털’ 신호와 유사하게 작동할 수 있음을 시사함으로써, 세포가 잡음(노이즈)을 활용해 스위치‑같은 결정을 내리는 메커니즘을 탐구하는 데도 기여한다.
**
댓글 및 학술 토론
Loading comments...
의견 남기기