A20이 NF‑κB 진동 주기를 조절한다: 삼중 피드백 루프의 새로운 기능
초록
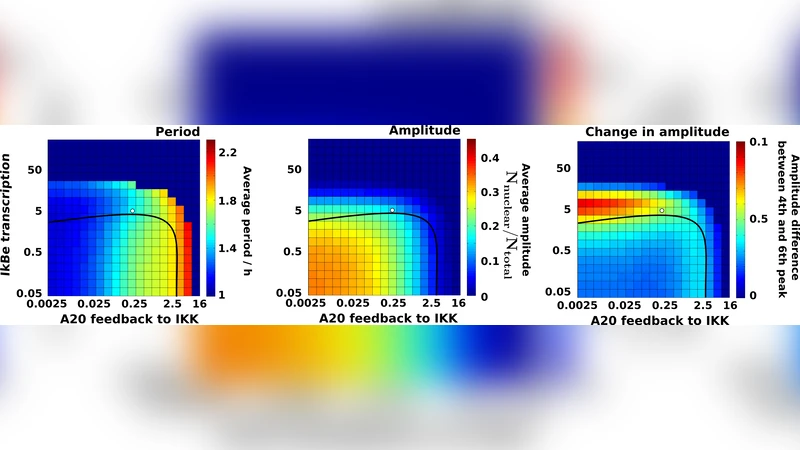
본 연구는 IkBa, IkBe, A20 세 가지 음성 피드백 루프를 포함한 수학 모델을 구축하여, A20이 진동을 감쇠시키는 동시에 핵 NF‑κB 진동 주기를 독립적으로 조절한다는 새로운 역할을 제시한다. 모델은 야생형 및 각 피드백 유전자 결손 마우스 세포의 실험 데이터를 재현하며, A20 발현을 siRNA 등으로 조절하면 진동 주기가 최대 2배까지 변할 수 있음을 예측한다.
상세 분석
이 논문은 NF‑κB 신호전달 경로의 핵-세포질 샤틀링이 1~2시간 주기의 감쇠 진동을 보인다는 실험적 사실을 이론적으로 재현하기 위해, 세 가지 주요 음성 피드백인 IkBa, IkBe, A20을 명시적으로 포함한 미분방정식 기반 모델을 제시한다. 기존 연구에서는 IkBa가 빠른 피드백을 제공해 진동을 유도하고, IkBe가 느린 피드백으로 진동을 억제한다는 점이 알려져 있었지만, A20의 역할은 아직 불분명했다. 저자들은 A20이 IKK 활성화를 억제하는 전사 후 조절 메커니즘을 모델에 반영함으로써, A20이 IkBe와 유사하게 진동을 감쇠시키지만, 그 감쇠 메커니즘이 시간 지연과 비선형 포화 효과를 통해 구현된다는 점을 발견했다. 특히, A20의 생산 속도와 분해율을 조절하면 핵 NF‑κB의 진동 주기가 크게 변한다는 것이 핵심 결과이다. 이는 피드백 루프가 ‘중첩된’ 구조를 이루어, 진폭 감소와 주기 조절을 독립적으로 다룰 수 있게 만든다. 모델 검증을 위해 WT, IkBa‑KO, IkBe‑KO, A20‑KO 세포주에서 TNF‑α 자극 후 NF‑κB 핵 이동 데이터를 시뮬레이션과 비교했으며, 모든 경우에서 실험적 곡선과 높은 상관관계를 보였다. 파라미터 스캔 결과, A20 발현이 0.5배에서 2배로 변할 때 진동 주기가 약 0.8배에서 1.9배로 변동함을 정량적으로 제시한다. 이러한 예측은 siRNA를 이용한 A20 억제 실험이나 과발현 실험을 통해 검증 가능하며, 신호 특이성 및 세포 유형에 따른 조절 메커니즘을 탐구하는 새로운 실험적 플랫폼을 제공한다. 논문은 또한 ‘피드백 네트워크 설계 원칙’으로서, 다중 피드백이 서로 다른 시간 스케일을 갖는 경우 시스템이 주기와 감쇠를 독립적으로 조절할 수 있음을 이론적으로 뒷받침한다. 이는 면역 반응, 염증성 질환, 암 등에서 NF‑κB 신호의 동적 특성을 조절하는 새로운 치료 전략을 구상하는 데 중요한 시사점을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기