알기닌‑다중펩타이드가 막을 파괴하고 일시적 구멍을 형성한다
초록
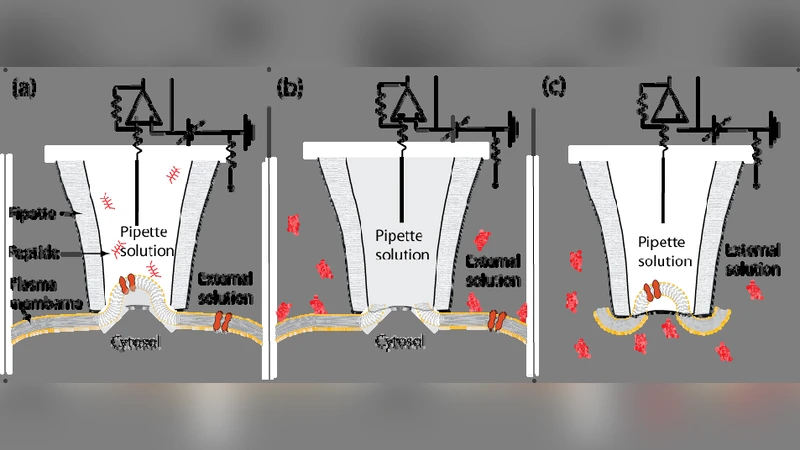
본 연구는 9개의 알기닌으로 구성된 Arg‑9 펩타이드가 전기적 구배 하에서 인공 인지질 이중층과 세포막에 일시적인 구멍을 만들고 이온 전류를 유도한다는 것을 분자동역학 시뮬레이션과 실험적으로 입증한다. 결과는 알기닌 잔기가 친수성임에도 불구하고 막 결합·불안정화에 핵심 역할을 하며, 세포 침투 펩타이드의 전이 메커니즘이 ‘pore formation’ 경로임을 시사한다.
상세 분석
이 논문은 기존에 HIV Tat 펩타이드가 알기닌 잔기의 전하와 수소결합을 이용해 인지질 이중층에 일시적인 구멍을 형성한다는 가설을 확장한다. 저자들은 9개의 연속된 알기닌(Arg‑9)으로 구성된 펩타이드를 선택해, 전기장 하에서의 행동을 전통적인 전자기학 모델과 원자 수준의 분자동역학(MD) 시뮬레이션으로 동시에 탐구하였다. 시뮬레이션 결과, Arg‑9는 먼저 막 표면에 전기적 끌어당김으로 강하게 부착하고, 알기닌의 양전하가 인산기와 형성하는 다중 수소결합이 국소적인 막 두께 감소와 지방산 사슬의 재배열을 유도한다. 이러한 구조적 교란은 막 내부에 물 분자와 이온이 침투할 수 있는 미세한 수분 채널을 형성하게 하며, 이는 전기적 구배가 존재할 때 지속적인 전류 흐름으로 관찰된다. 실험적으로는 planar lipid bilayer 장치와 두 종류의 세포(골육종 세포, 제대동맥 평활근 세포)를 이용해 전압을 가했을 때 Arg‑9가 유도하는 전류의 크기와 지속 시간을 측정하였다. 전류는 전압에 비례적으로 증가했으며, 전압이 제거되면 전류가 급격히 사라지는 ‘전압 의존성 일시적 구멍’ 특성을 보였다. 또한, 구멍의 평균 직경은 약 0.5–1 nm 수준으로 추정되었으며, 이는 알기닌의 사이드 체인 길이와 일치한다. 중요한 점은 Arg‑9가 단일 알기닌이 아닌 연속된 다중 알기닌으로 구성될 때, 전하 밀도가 충분히 높아져 막에 대한 결합 에너지가 크게 증가하고, 따라서 구멍 형성 확률이 급격히 상승한다는 것이다. 이와 같은 결과는 기존의 ‘직접 침투’ 모델(막을 통과하는 펩타이드가 완전한 구조 변화를 겪는다)과 대비해, ‘전기장 유도 일시적 구멍(pore formation)’ 모델이 알기닌 풍부 펩타이드의 세포 침투 메커니즘을 설명하는 데 더 적합함을 시사한다.
댓글 및 학술 토론
Loading comments...
의견 남기기