샤논 엔트로피 추정에 제임스‑스틴 수축법 적용 및 유전자 연관 네트워크 구축
본 논문은 표본이 매우 적은 고차원 범주형 데이터에서 엔트로피와 상호정보량을 정확히 추정하기 위해 제임스‑스틴(James‑Stein) 수축 추정기를 제안한다. 균일 분포를 목표로 하는 수축 강도 λ를 데이터‑드리븐 방식으로 결정하고, 이를 셀 빈도에 적용한 뒤 샤논 엔트로피 공식에 대입한다. 시뮬레이션에서 기존의 8가지 추정법(NBS, Chao‑Shen 등)보다 평균제곱오차와 편향 면에서 우수함을 보였으며, 계산 속도도 수천 배 빠르다. 마지막…
저자: Jean Hausser, Korbinian Strimmer
본 논문은 고차원 범주형 데이터에서 엔트로피와 상호정보량을 정확히 추정하는 새로운 방법을 제시한다. 전통적인 최대우도(ML) 추정은 표본 수가 변수 차원보다 현저히 작을 때(‘small n, large p’) 빈도가 0인 셀을 무시하게 되며, 이로 인해 엔트로피가 크게 과소평가된다. Miller‑Madow와 같은 1차 편향 보정도 충분히 개선되지 못한다. 베이지안 접근법은 Dirichlet 사전으로 가짜 카운트를 추가해 분산을 감소시키지만, 사전 파라미터 선택이 주관적이며 부적절하면 오히려 성능이 저하된다. 최근에는 NSB와 Chao‑Shen이 복잡한 사전 구조와 Good‑Turing 보정을 통해 통계적 효율성을 높였지만, 계산 비용이 크고 구현이 복잡한 단점이 있다.
이에 저자들은 제임스‑스틴(James‑Stein) 수축 아이디어를 엔트로피 추정에 적용한다. 두 개의 추정 모델, 즉 편향은 0이지만 분산이 큰 ML 추정과 편향은 크지만 분산이 작은 균일 분포를 선형 결합한다. 구체적으로 ˆθ_shrinkₖ=λ tₖ+(1‑λ) ˆθ_MLₖ (tₖ=1/p) 로 정의하고, λ는 데이터에 의해 자동으로 결정된다. λ̂는 전체 분산 대비 목표와 관측 빈도 차이의 제곱합 비율로 계산되는 식(5)에서 얻으며, 이는 사전 가중치를 데이터‑드리븐 방식으로 추정하는 경험적 베이지안과 동일한 형태이다. 따라서 사전 파라미터 A를 별도로 지정할 필요 없이 관측 데이터가 직접 수축 강도를 결정한다.
수축된 빈도 ˆθ_shrinkₖ를 샤논 엔트로피 공식에 대입하면 ˆH_shrink이 얻어지며, 이는 셀 빈도와 엔트로피를 동시에 제공한다는 점에서 기존 추정법보다 실용성이 높다. 저자들은 p=1000으로 고정하고, n을 10부터 10 000까지 변화시키며 네 가지 확률 분포 시나리오(극히 희소 Dirichlet, 균일 Dirichlet, 절반 구조적 영, Zipf)를 사용해 1 000번씩 시뮬레이션을 수행했다. 각 시뮬레이션에서 셀 빈도와 엔트로피의 평균제곱오차(MSE)와 편향을 계산하였다.
시뮬레이션 결과는 다음과 같다. (1) 표본이 충분히 큰 경우 모든 추정기가 좋은 성능을 보인다. (2) ML과 Miller‑Madow는 대부분의 시나리오에서 가장 큰 편향과 MSE를 보이며, 특히 중간 규모 표본에서도 부적절하다. (3) 최소극대(minimax)와 1/p 베이지안은 약간 개선되지만 큰 차이는 없다. (4) 1/2와 1 사전 파라미터를 갖는 베이지안 추정은 시나리오 2·3에서는 우수하지만, 희소 분포(시나리오 1)와 Zipf(시나리오 4)에서는 성능이 급격히 떨어진다. (5) NSB, Chao‑Shen, 그리고 제안된 수축 추정기는 모든 시나리오와 표본 크기에서 낮은 MSE와 거의 무편향을 유지한다. 특히 수축 추정기는 NSB와 동일한 통계적 효율성을 보이면서도 실행 시간이 약 1 000배 빠르다.
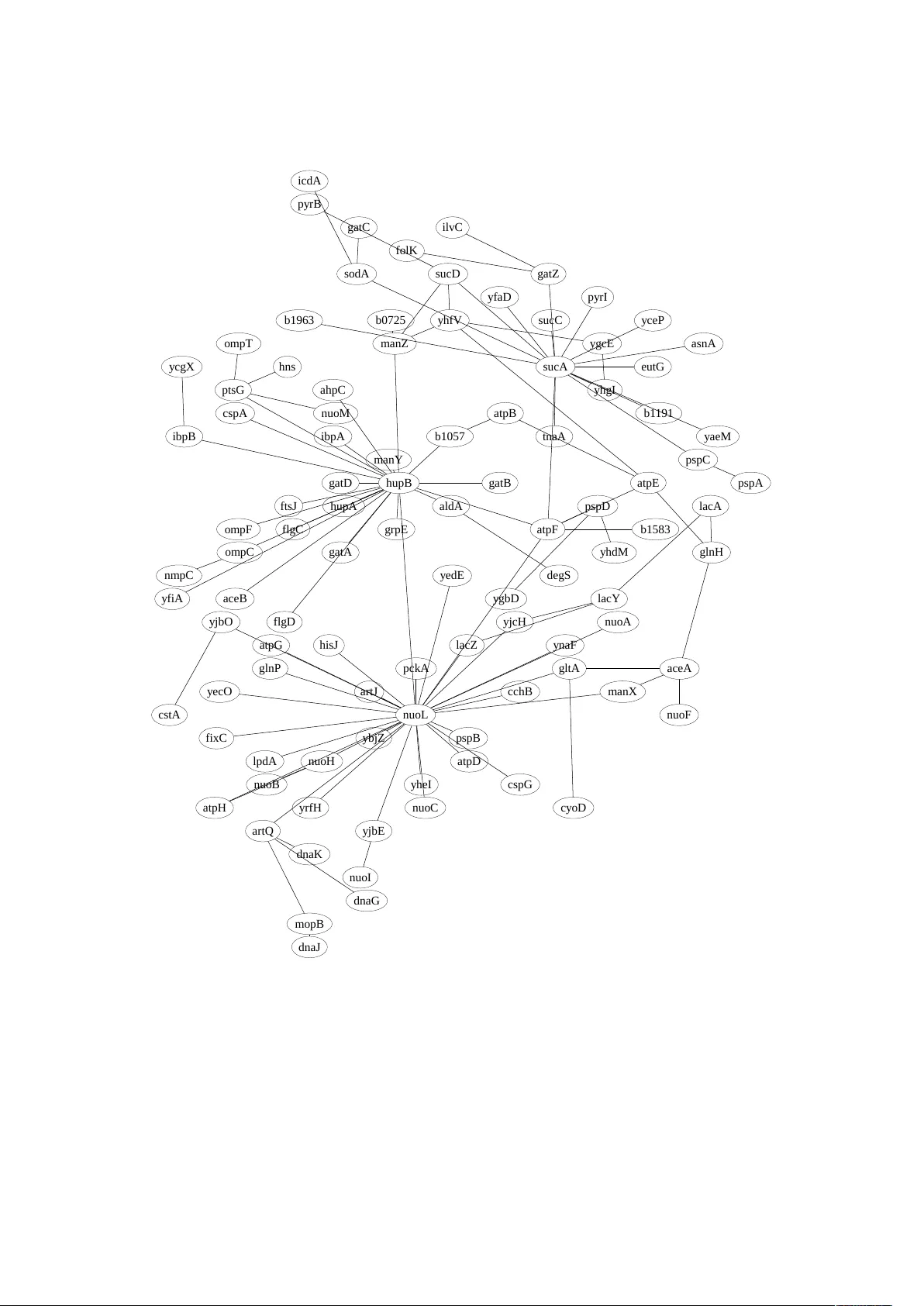
실제 데이터 적용으로 저자들은 E. coli 유전자 발현 데이터를 사용해 각 유전자 쌍의 상호정보량을 추정하고, ARACNE·MRNET과 유사한 임계값 기반 비선형 유전자 연관 네트워크를 구축했다. 수축 추정기로 얻은 엔트로피와 상호정보량은 기존 방법보다 더 많은 유의미한 연결을 식별했으며, 계산 효율성 덕분에 대규모 유전체 데이터에서도 실시간 분석이 가능함을 입증했다. 또한, 제공된 R 패키지는 사용자가 손쉽게 수축 추정기를 적용할 수 있도록 설계되었다.
결론적으로, 제임스‑스틴 수축 추정기는 “small n, large p” 상황에서 엔트로피와 상호정보량을 정확히 추정하는 데 있어 통계적 효율성, 계산 속도, 구현 용이성 측면에서 기존 방법들을 능가한다. 특히 고차원 유전학, 신경과학, 이미지 분석 등 표본이 제한된 분야에서 널리 활용될 수 있는 강력한 도구로 평가된다.
원본 논문
고화질 논문을 불러오는 중입니다...
댓글 및 학술 토론
Loading comments...
의견 남기기