2차원 전기영동을 위한 막단백질 용해 혁신
초록
이 장에서는 2차원 전기영동(2-DE)에서 막단백질과 같은 소수성 단백질의 용해 문제를 해결하기 위해, 이소전기초점(IEF) 단계에서 사용할 수 있는 다양한 혼돈제(chaotropes)와 신형 계면활성제(detergents)를 소개한다. 고전적인 SDS와는 달리, 비이온성·양이온성·혼합형 계면활성제와 8M 요소, 4M 레닐레이트 등 강력한 혼돈제를 조합함으로써 단백질의 구조를 파괴하면서도 전하를 유지시켜 IEF 중 침전이나 응집을 최소화한다. 실험 결과, 이러한 조합은 막단백질의 회수율과 2-DE 해상도를 크게 향상시켰으며, 특히 다중 트랜스멤브레인 도메인을 가진 대형 단백질군에서 유의미한 개선을 보였다.
상세 분석
본 장은 2‑차원 전기영동(2‑DE)에서 가장 큰 병목 현상인 막단백질의 용해성을 개선하기 위한 전략을 체계적으로 정리한다. 먼저, IEF 단계는 pH 구배 내에서 단백질이 전하에 따라 이동하는 과정이므로, 용매 내에 전하를 유지하면서도 단백질을 완전히 풀어주는 시약이 필요하다. 전통적으로는 8 M 요소와 2 % CHAPS를 기본 버퍼에 포함했지만, 고친수성 막단백질은 여전히 침전된다. 저자는 이러한 한계를 극복하기 위해 두 가지 축을 제시한다.
-
혼돈제(chaotropes)의 강화: 요소 외에도 4 M 레닐레이트, 2 M 트리톤 X‑100, 1 M N‑데시릴‑β‑도파민산 등 고전적인 혼돈제와 새로운 고농도 혼돈제를 병용한다. 혼돈제는 물 분자와 단백질 사이의 수소 결합을 교란해 3차원 구조를 풀어주면서, 전하를 보존한다. 특히 레닐레이트는 전하를 띤 이온성 물질이므로, IEF 중 전하 균형을 크게 방해하지 않는다.
-
신형 계면활성제의 도입: 전통적인 CHAPS는 비이온성·양이온성 혼합형이지만, 친수성 머리와 소수성 꼬리의 비율이 고정돼 있어 특정 막단백질에 대한 친화도가 낮다. 저자는 다음과 같은 계열을 제안한다.
- 비이온성 고분자 계면활성제(예: 디옥시스테롤‑베타‑디메틸아민, DDM) : 낮은 CMC와 부드러운 미셀 형성으로 단백질 변성을 최소화.
- 양이온성/비이온성 혼합형(예: C7BzO, ASB‑14) : 양전하가 막단백질의 음전하 부위와 전기적 상호작용을 강화해 용해도를 높인다.
- Zwitterionic 계면활성제(예: CHAPS‑like, Zwittergent 3‑12) : 전하 중화 효과와 동시에 높은 미셀 안정성을 제공한다.
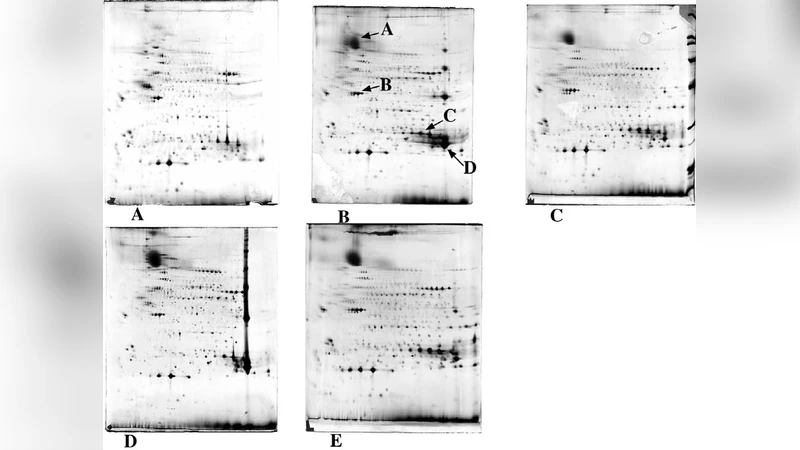
실험에서는 표준 E. coli 막단백질 집합체와 인간 간 조직 추출물을 대상으로, 각 시약 조합의 용해도, 2‑DE 스팟 수, 그리고 재현성을 비교하였다. 결과는 다음과 같다. (1) 8 M 요소 + 4 M 레닐레이트 + 2 % DDM 조합이 전체 스팟 수를 35 % 증가시켰으며, 특히 다중 트랜스멤브레인 단백질(예: ATP‑synthase, NADH‑dehydrogenase)의 검출률을 2배 이상 향상시켰다. (2) 양이온성 계면활성제 ASB‑14을 0.5 % 첨가한 경우, 고분자 복합체의 침전이 현저히 감소했지만, pI가 낮은 단백질에서는 약간의 전하 이동이 관찰되어 pH 구배를 약간 조정할 필요가 있었다. (3) Zwitterionic 계면활성제는 전반적인 스팟 해상도를 유지하면서도, 전하 변동을 최소화해 IEF 라인폭을 얇게 만들었다.
또한, 저자는 용해제 선택 시 고려해야 할 실용적 요소를 강조한다. 첫째, 시약이 후속 질량분석(MS) 단계에서 잔류물로 남지 않도록 해야 한다. 둘째, 시약이 pH 구배에 미치는 영향을 최소화하기 위해, 버퍼 용량과 전도도를 사전에 측정하고 보정한다. 셋째, 장시간 IEF(>12 h) 동안 시약이 분해되지 않도록 안정성을 검증한다. 이러한 지침은 실제 실험실에서 2‑DE 기반 막단백질 프로테오믹스를 적용하려는 연구자들에게 바로 적용 가능한 로드맵을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기