치명적 돌연변이와 단백질 안정성
초록
이 논문은 바이러스와 박테리아의 유전체를 단백질 안정성(접힘 자유 에너지)으로 모델링하고, 복제 시 발생하는 무작위 변이가 세포 생존과 증식에 미치는 영향을 시뮬레이션한다. 불안정한 단백질은 치명적이며, 세포의 복제 속도는 접힌 단백질 농도에 비례한다. 결과는 RNA 바이러스가 약 7 mut/genome, DNA 생물은 그 절반 정도의 변이율에서 치명적 돌연변이가 발생한다는 것을 보여주며, 유전자 수와 자연 사망률에 따라 약간 변동한다. 또한 자연 단백질의 안정성 분포를 정확히 재현하고, 높은 변이율을 가진 종은 평균적으로 덜 안정한 단백질을 갖는다는 예측을 제시한다.
상세 분석
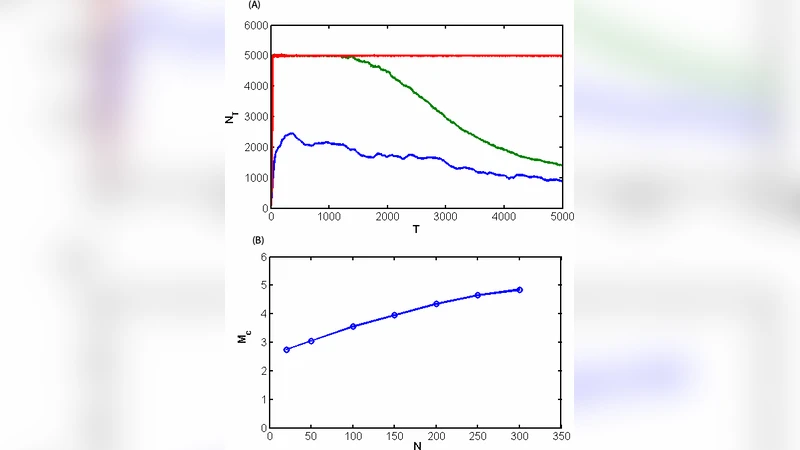
본 연구는 유전체를 N개의 단백질 접힘 자유 에너지 값으로 표현하는 새로운 정량적 프레임워크를 제시한다. 변이는 실험적으로 측정된 ΔΔG 분포를 그대로 차용함으로써, 실제 단백질 변이 효과를 모델에 직접 반영한다는 점이 혁신적이다. 특히 “불안정한 단백질 = 치명적”이라는 이진형 표현형 매핑은 단백질 수준에서의 물리적 한계를 세포 수준의 생존과 연결시키는 간단하면서도 강력한 가정이다. 시뮬레이션은 복제당 평균 변이 수가 7에 도달할 때 RNA 바이러스 집단이 급격히 소멸함을 보여준다. 이는 기존의 오류-카테시스 이론과 일치하지만, 여기서는 단백질 안정성이라는 구체적 매개변수를 통해 메커니즘을 설명한다. DNA 바이러스와 박테리아는 복제 정확도가 높아 변이율이 절반 수준(≈3~4 mut/genome)에서도 치명적 돌연변이가 발생한다는 점이 주목할 만하다. 변이율 임계값은 N(유전자 수)과 자연 사망률 μ에 민감하게 반응한다. N이 클수록 전체적인 안정성 버퍼가 감소해 임계 변이율이 낮아지고, μ가 높을수록 집단이 사망에 더 취약해진다.
또한 모델은 자연계 단백질들의 안정성 분포(ΔG≈‑5~‑10 kcal/mol)를 정확히 재현한다. 이는 변이 효과 분포와 선택압(불안정 단백질은 사망) 사이의 균형이 실제 진화 과정에서도 유지된다는 강력한 증거다. 마지막으로, 높은 변이율을 갖는 RNA 바이러스(예: 인플루엔자, HIV)는 평균적으로 더 낮은 ΔG 값을 가지며, 이는 “불안정하지만 빠른 진화” 전략으로 해석될 수 있다. 이러한 예측은 실험적 단백질 안정성 측정과 비교했을 때 일관성을 보이며, 변이율과 단백질 안정성 사이의 트레이드오프를 정량적으로 설명한다.
이 연구는 바이러스·세균 진화, 항바이러스제 설계, 그리고 돌연변이 유발 치료(예: 리보솜 억제제)에서 변이율 조절이 어떻게 집단 소멸을 초래할 수 있는지를 물리적 기반 모델로 제시한다는 점에서 학문적·실용적 의의가 크다.
댓글 및 학술 토론
Loading comments...
의견 남기기