초감도 나노기계식 캔틸레버를 이용한 반코마이신‑뮤코펩타이드 결합 탐지
초록
본 연구는 라벨‑프리 나노기계식 캔틸레버 배열을 활용해 반코마이신이 세균 세포벽 전구체인 뮤코펩타이드와 결합하는 현상을 10 nM 수준의 감도와 혈청 내 임상적 농도에서 실시간으로 검출하였다. 민감형과 내성형 뮤코펩타이드 유사체의 결합 상수 차이를 정량화하고, 표면 응력 발생 메커니즘을 ‘화학 결합 인자’와 ‘기하학적 연결 인자’의 결합으로 보는 퍼콜레이션 모델로 설명하였다. 이 결과는 BioMEMS 기반 진단·감시 플랫폼의 설계와 항생제 작용 메커니즘 이해에 새로운 패러다임을 제시한다.
상세 분석
이 논문은 마이크로전기기계시스템(MEMS) 기술을 항생제–표적 상호작용 연구에 적용한 선구적인 사례로, 특히 반코마이신과 그 표적인 D‑알라닌‑D‑알라닌(D‑Ala‑D‑Ala) 구조를 모방한 뮤코펩타이드 유사체 사이의 결합을 캔틸레버 기반 표면 응력 측정을 통해 정량화하였다. 기존의 SPR, ITC 등 전통적인 바이오센서와 달리 캔틸레버는 라벨이 필요 없으며, 미세한 표면 응력 변화를 전기적 신호로 변환해 10 nM 이하의 결합 농도를 감지한다. 특히 혈청과 같은 복잡한 매트릭스에서도 신호 대 잡음비가 충분히 높아 실제 임상 샘플 분석이 가능함을 입증했다.
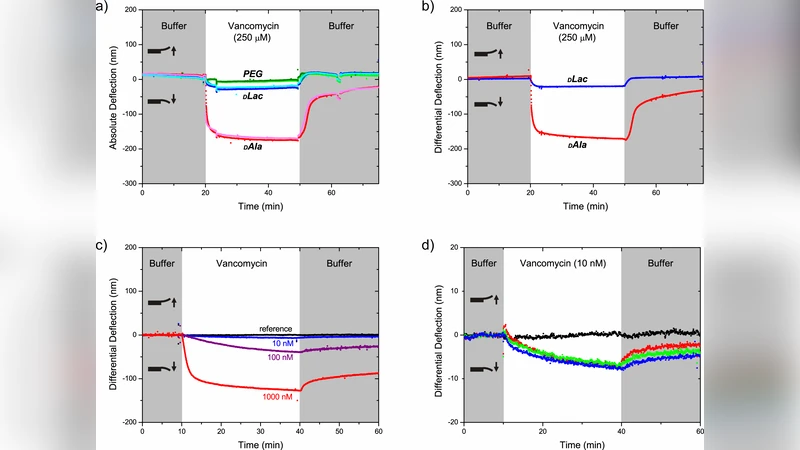
연구팀은 두 종류의 뮤코펩타이드를 설계했는데, 하나는 반코마이신에 친화적인 D‑Ala‑D‑Ala 말단을 보유한 ‘민감형’, 다른 하나는 D‑Ala‑D‑Lac(락트산) 변이를 도입해 결합 친화도가 크게 감소한 ‘내성형’이다. 캔틸레버 표면에 이들 펩타이드를 다양한 밀도로 자기조립시킨 뒤, 반코마이신 농도에 따른 응력 변화를 측정했다. 응력-농도 곡선으로부터 각각의 결합 상수(K_D)를 추정했으며, 민감형은 약 0.5 µM, 내성형은 30 µM 수준으로 차이가 뚜렷했다. 이는 기존의 미세플레이트 기반 결합 실험과 일치하면서도, 실시간·라벨프리 방식이라는 장점을 제공한다.
가장 혁신적인 부분은 표면 응력 발생 메커니즘을 ‘퍼콜레이션(percolation)’ 모델로 해석한 것이다. 저자들은 응력이 단순히 개별 결합에 의해 발생하는 것이 아니라, 결합된 분자들이 형성하는 네트워크가 기계적으로 연결될 때 전체 캔틸레버에 전달된다고 가정했다. 이를 수학적으로는 화학 결합 인자(결합당 발생하는 미세 응력)와 기하학적 연결 인자(결합된 분자들의 공간적 연속성, 즉 퍼콜레이션 임계치)를 곱한 형태로 표현했다. 실험적으로는 뮤코펩타이드 밀도를 조절함으로써 퍼콜레이션 임계점을 탐색했으며, 일정 밀도 이하에서는 응력 신호가 거의 없고, 임계치를 초과하면 급격히 신호가 증폭되는 비선형 특성을 확인했다. 이러한 현상은 기존의 표면 응력 모델(예: Stoney 방정식 기반)에서는 설명되지 않으며, 나노스케일에서의 기계적 연결성이 화학 반응과 결합해 새로운 감지 메커니즘을 만든다는 점에서 학문적·기술적 의미가 크다.
퍼콜레이션 개념을 도입함으로써 향후 BioMEMS 디바이스 설계에 두 가지 전략적 시사점을 제공한다. 첫째, 표면에 고밀도·고정밀 패턴을 구현해 퍼콜레이션 임계치를 낮추면 감지 한계가 현저히 개선된다. 둘째, 캔틸레버 자체의 기계적 특성(탄성계수, 두께 등)을 최적화해 응력 전달 효율을 높이면, 초저농도(피코몰 수준)까지도 검출 가능해진다. 또한, 이 모델은 항생제와 세포벽 전구체 사이의 결합이 실제 살아있는 박테리아에서 어떻게 전파되는지를 이해하는 데도 활용될 수 있다. 예를 들어, 박테리아 표면에 존재하는 D‑Ala‑D‑Ala 사슬이 일정 밀도 이상으로 배열될 때만 반코마이신이 효과적으로 작용한다는 가설을 검증하는 실험적 기반을 제공한다.
결론적으로, 이 연구는 나노기계식 캔틸레버를 이용한 라벨프리 바이오센서가 항생제 감지와 저항성 메커니즘 분석에 강력한 도구가 될 수 있음을 입증했으며, 퍼콜레이션 기반 응력 모델은 향후 초감도 바이오디텍터 설계와 항생제 작용 메커니즘 연구에 새로운 패러다임을 제시한다.
댓글 및 학술 토론
Loading comments...
의견 남기기