구속과 군집이 모델 단백질 접힘에 미치는 영향
초록
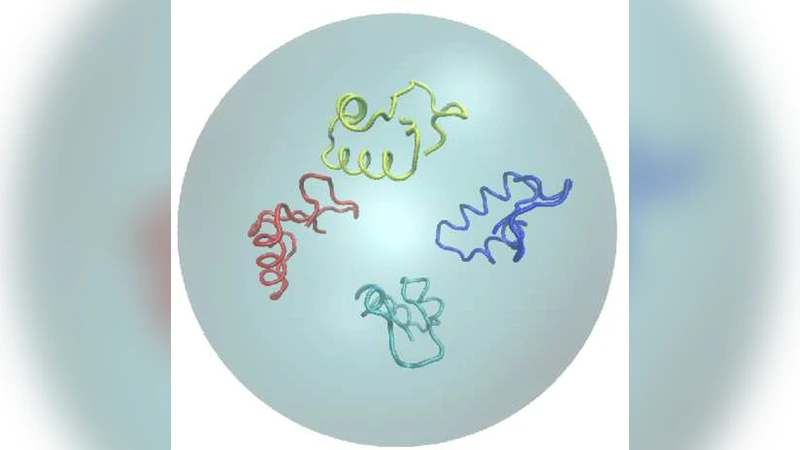
본 연구는 부드러운 반발 구 안에 배치된 크램빈 모델 단백질을 분자동역학 시뮬레이션으로 조사한다. 구속은 최적 온도에서 접힘 속도를 약간 늦추고 경로를 변화시키지만 큰 차이는 없다. 여러 단백질을 동시에 넣어 군집 효과를 살펴보면, 순수한 부피 배제 효과만 존재할 경우 단일 단백질과 동일한 접힘 시간을 보인다. 그러나 단백질 간 인력 상호작용이 단일 접힘 접촉 강도의 절반 이상이면 접힘이 방해되고, 강도가 클수록 응집·오접힘이 증가한다.
상세 분석
이 논문은 거시적인 생물학적 환경을 단순화한 구형 구속 공간과 군집 상황을 통해 단백질 접힘 역학을 탐구한다. 저자들은 코스테인(coarse‑grained) 모델을 사용해 46개의 아미노산으로 구성된 크램빈(crambin)을 구현했으며, 구의 반경 R을 조절해 다양한 구속 정도를 시뮬레이션했다. 구속이 존재하면 자유 에너지 지형이 변형돼, 전이 상태의 자유 에너지 장벽이 약간 상승하고, 따라서 최적 온도(T_opt)에서의 접힘 속도가 감소한다. 그러나 이 감소는 수십 퍼센트 수준에 머물러, 구속 자체가 접힘 메커니즘을 근본적으로 바꾸지는 않는다.
군집 효과를 조사하기 위해 동일한 크기의 단백질 N개를 구 안에 넣고, 초기에는 완전히 변성된 상태(전부 펼쳐진)에서 재접힘을 시작한다. 여기서 두 가지 상호작용 시나리오를 설정했다. 첫 번째는 순수한 부피 배제(soft‑repulsive)만을 고려한 경우로, 이는 실제 세포질에서 물질이 차지하는 공간을 모사한다. 결과는 단일 단백질과 거의 동일했으며, 접힘 시간은 단백질 수에 비례하지 않고, 오히려 약간의 가속 효과가 관찰되었다. 이는 주변 단백질이 일시적인 “템플릿” 역할을 해, 접힘 경로를 제한하고 효율을 높일 수 있음을 시사한다.
두 번째 시나리오는 단백질 간 인력(예: 수소 결합, 반데르발스 상호작용)을 추가한 경우이다. 인력 강도 ε_inter을 단일 단백질 내부 접촉 강도 ε_intra의 비율로 조정했으며, ε_inter/ε_intra ≈ 0.5를 초과하면 접힘이 현저히 지연된다. 인력이 강할수록 단백질 간 비특이적 결합이 형성돼, 올바른 토폴로지를 방해하고, 결국 응집(aggregation) 혹은 오접힘(misfolding)으로 이어진다. 특히 ε_inter/ε_intra ≈ 0.8 이상에서는 대부분의 시뮬레이션이 정상적인 네이티브 구조에 도달하지 못하고, 큰 클러스터를 형성한다. 이는 세포 내 고농도 단백질 환경에서, 비특이적 상호작용을 억제하는 샤페론(chaperone)이나 이온 강도 조절이 왜 중요한지를 물리적으로 뒷받침한다.
또한, 저자들은 접힘 경로 분석을 통해 구속이 있는 경우 초기 접힘 단계에서 “핵심 부위”(core region)의 형성이 더 빠르게 일어나지만, 전체 구조가 완성되기 전까지는 구의 경계와의 충돌이 잦아, 최종 네이티브 상태에 도달하는 데 추가적인 재배열이 필요함을 확인했다. 군집 상황에서는 단백질 간 충돌이 빈번해, 초기 핵심 형성 단계가 지연될 수 있지만, 부피 배제만 있을 때는 이러한 충돌이 오히려 구조적 정렬을 촉진한다는 역설적인 결과가 도출되었다.
전반적으로 이 연구는 단백질 접힘을 이해하는 데 있어 물리적 구속과 군집이라는 두 환경 요인이 독립적이면서도 상호작용한다는 점을 명확히 보여준다. 구속은 접힘 속도를 약간 늦추지만, 경로 자체는 크게 변하지 않으며, 순수한 부피 배제는 다중 단백질 시스템에서도 효율적인 접힘을 가능하게 한다. 반면, 비특이적 인력은 임계값을 넘어설 경우 접힘을 방해하고 응집을 촉진한다는 점에서, 세포 내 단백질 품질 관리 메커니즘의 필요성을 강조한다.
댓글 및 학술 토론
Loading comments...
의견 남기기