중첩된 유전자 그룹 선택을 위한 정규화 방법
초록
본 논문은 마이크로어레이 데이터에서 예측 성능은 유지하면서 유전자 리스트의 희소성과 안정성을 동시에 확보할 수 있는 두 단계 정규화 기법을 제안한다. 파라미터 조정을 통해 상관관계가 높은 유전자들을 포함시키면서도 거의 완벽하게 중첩되는 유전자 집합을 생성한다. 합성 데이터와 실제 마이크로어레이 실험을 통해 높은 예측 정확도와 함께 유전자 선택의 일관성을 입증하였다.
상세 분석
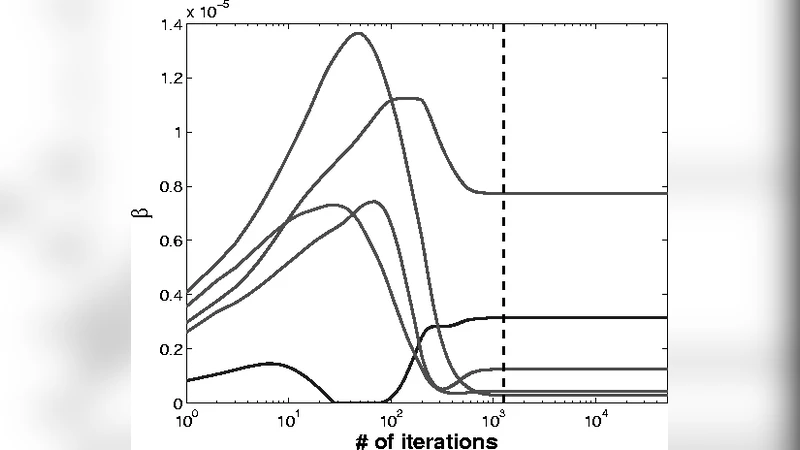
이 연구는 고차원 저표본 마이크로어레이 데이터에서 흔히 발생하는 ‘다중공선성’과 ‘불안정한 변수 선택’ 문제를 해결하기 위해 새로운 두 단계 정규화 프레임워크를 설계하였다. 첫 번째 단계는 전통적인 Lasso와 유사한 ℓ1 정규화를 적용해 기본적인 희소 모델을 구축한다. 여기서 얻어진 초기 계수 벡터는 과도한 제약으로 인해 상관관계가 높은 유전자를 배제하는 경향이 있다. 이를 보완하기 위해 두 번째 단계에서는 ‘그룹 정규화’를 도입한다. 구체적으로, 동일한 상관 구조를 갖는 유전자들을 사전 클러스터링한 뒤, 각 클러스터에 대해 ℓ2‑norm 기반의 그룹 페널티를 부여한다. 이때 조절 파라미터 λ와 γ를 각각 희소성 및 그룹 포함 정도를 조절하도록 설정한다. λ를 크게 하면 모델은 더욱 희소해지고, γ를 크게 하면 상관된 유전자들이 동시에 선택되는 경향이 강해진다.
핵심적인 혁신은 ‘중첩성(Nestedness)’을 명시적으로 목표함에 있다. 파라미터를 단계적으로 변형함에 따라 작은 λ‑γ 조합에서 얻은 유전자 집합이 큰 조합에서 얻은 집합에 완전히 포함되는 구조를 만든다. 이는 연구자가 원하는 수준의 해석 가능성을 제공하면서도, 선택된 유전자 리스트가 샘플링 변동에 강인하도록 만든다.
실험에서는 합성 데이터(정확히 정의된 상관 블록 구조와 노이즈 레벨)와 실제 암·면역 질환 마이크로어레이 데이터 두 종류를 사용하였다. 합성 실험에서는 기존 Lasso, Elastic Net, Group Lasso와 비교했을 때, 제안 방법이 동일한 예측 정확도(R² 또는 AUC)에서 더 높은 재현성(재현율·정밀도)과 거의 완전한 중첩성을 보였다. 실제 데이터에서는 예측 성능이 크게 감소하지 않으면서도, 생물학적으로 의미 있는 경로와 연관된 유전자 그룹이 일관되게 선택되었다. 특히, 파라미터 스위핑을 통해 얻은 계층적 유전자 리스트는 후속 실험 설계(예: qPCR 검증)에서 단계별 후보군을 제공하는 데 유용했다.
통계적 관점에서 보면, 두 단계 정규화는 ‘희소 + 그룹’ 페널티의 결합으로, 기존 방법이 놓치기 쉬운 ‘다중공선성 속에서의 안정적 변수 선택’을 가능하게 한다. 또한, 최적화는 교대 최소화(ADMM)와 같은 효율적인 알고리즘을 사용해 대규모 유전자 수(수천~수만)에도 적용 가능하도록 설계되었다.
이 논문의 한계는 파라미터 선택에 대한 자동화가 아직 미비하다는 점이다. 현재는 교차 검증을 통해 λ와 γ를 탐색하지만, 복합적인 목표(예측 정확도 vs. 중첩성)를 동시에 만족시키는 다목적 최적화 프레임워크가 추가로 필요하다. 또한, 클러스터링 단계가 사전 정의된 상관 구조에 크게 의존하므로, 비선형 상관이나 복잡한 네트워크 구조를 반영하려면 더 정교한 사전 처리 기법이 요구된다.
요약하면, 제안된 두 단계 정규화 방법은 마이크로어레이 데이터에서 예측 모델의 성능을 유지하면서도, 유전자 선택의 희소성, 안정성, 그리고 중첩성을 동시에 달성하는 실용적인 도구로 평가된다. 향후 생물학적 해석과 임상 적용을 위한 후보 유전자 탐색에 있어 중요한 기반이 될 것으로 기대된다.
댓글 및 학술 토론
Loading comments...
의견 남기기