혼돈 유도 종양 성장 모델: 다중 규모 확산 모델에 비선형 결합을 도입한 새로운 접근
초록
본 논문은 기존 다중 규모 확산 암 침윤 모델(MDCM)에 네 개의 비선형 결합 파라미터(α, β, γ, δ)를 추가하여, 종양 세포, 매트릭스 메탈로프로테아제, 매트릭스 분해 효소, 산소 농도 사이에 로렌츠형 혼돈 끌개를 형성한다. 공간 미분을 무시한 시간 전역 ODE 시스템에서 라오즈 스트레인저 어트랙터와 유사한 궤적을 보이며, 초기 조건과 파라미터에 대한 민감한 의존성을 입증한다. 수정된 PDE 형태에서도 이 혼돈 구조가 유지된다고 주장하며, 암 발생·전이 과정의 불확실성을 수학적으로 설명하고, 혼돈 제어 기반 치료 전략을 제시한다.
상세 분석
본 연구는 먼저 기존 MDCM(다중 규모 확산 암 침윤 모델)의 4차원 연속‑이산 하이브리드 구조를 재검토한다. 원래 모델은 종양 세포 밀도 n, 매트릭스 메탈로프로테아제(f), 매트릭스 분해 효소(m), 산소(c) 네 변수에 대해 확산·화학반응·하프토시스 항을 포함한 PDE 시스템(식 1‑4)을 제시한다. 저자들은 이 시스템을 비차원화하고, 공간 미분을 완전히 제거하여 순수 시간 전역 ODE(식 12‑15)로 축소한다. 그러나 이 단순화된 형태는 변수 간 비선형 결합이 거의 없으며, 시뮬레이션 결과 거의 선형적인 시간 변화를 보인다.
이에 저자들은 네 개의 새로운 파라미터 α, β, γ, δ를 도입해 ODE를 재구성한다(식 16‑19). 구체적으로 α는 종양 세포 부피(증식/비증식 비율), β는 포도당 수준, γ는 종양 세포 수, δ는 표면 확산(포화 수준)을 의미한다. 새로운 항들은 f와 m, c 사이에 교차 피드백을 만들고, 특히 식 (17)에서 f와 m의 차이에 αη를 곱함으로써 매트릭스‑효소 상호작용을 강화한다. 식 (18)에서는 βκn와 f(γ−c)−m 형태로 비선형 결합을 도입해 종양 세포와 산소 농도의 상호 의존성을 강조한다. 식 (19)에서는 ν f m와 ω n, δφc가 동시에 작용해 산소 생산·소모 메커니즘을 복합적으로 조절한다.
이러한 비선형 구조는 로렌츠 시스템과 유사한 삼차원 서브스페이스(f‑m‑c)에서 스트레인저 어트랙터를 생성한다. 파라미터 값을 α=0.06, β=0.05, γ=26.5, δ=40으로 설정하고 초기 조건을 동일하게 유지했을 때, 시뮬레이션은 전통적인 주기적 궤적이 아닌, 복잡한 꼬리와 프랙탈 차원을 갖는 궤적을 보여준다(그림 1‑4). 저자들은 파라미터를 소폭 변동시켜도 정성적 혼돈 특성은 유지된다고 보고, 모델이 실제 종양 성장의 불확실성·예측 불가능성을 반영한다는 주장을 뒷받침한다.
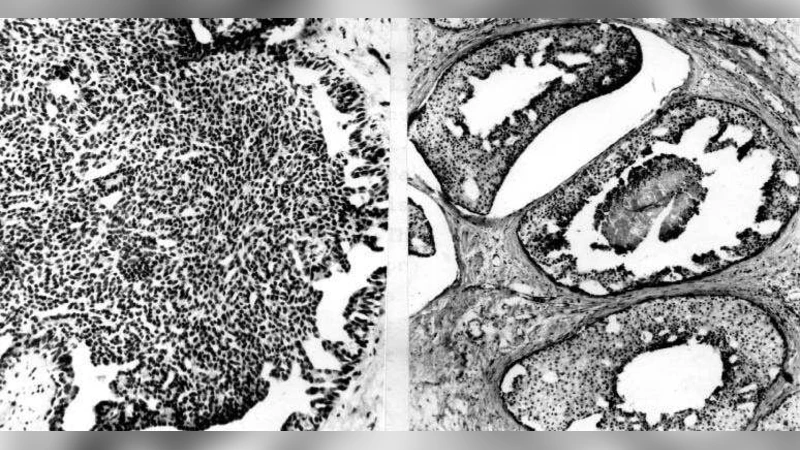
수학적 분석 외에도 생물학적 해석을 제공한다. α는 증식‑비증식 비율로, 종양 성장 단계에 따라 변할 수 있는 세포 주기 동역학을 반영한다. β는 종양 미세환경의 포도당 공급을, γ는 종양 전체 세포 수를, δ는 조직 내 확산 제한을 나타낸다. 이러한 파라미터와 혼돈 현상의 연관성을 통해, 종양의 형태학적 변형, 염색체 구조 변화(p27, SATB1 등)와도 연결짓는다. 특히, 고수준의 크로마틴 변형이 높은 혼돈 강도와 연관될 수 있음을 제시한다.
마지막으로, 저자들은 혼돈 제어(OGY 방법, 안티‑컨트롤)와 같은 이론적 도구를 암 치료에 적용할 가능성을 논의한다. 세포 재교육, p27 활성화, SATB1 억제 등은 모델 파라미터를 조절해 혼돈을 억제하거나 원하는 동역학으로 전환시킬 수 있는 잠재적 전략으로 제시된다. 전체적으로, 이 논문은 기존 확산‑반응 모델에 비선형 결합을 도입해 혼돈 이론을 암 성장·전이 연구에 통합하려는 시도이며, 수학·생물학·임상 사이의 다학제적 연결 고리를 모색한다.
댓글 및 학술 토론
Loading comments...
의견 남기기