대장균 lac 오페론 유도에서 이중안정성 결정 요인
초록
본 연구는 외부 포도당이 없는 조건에서 인공 유도제와 천연 유도제(락토스) 각각에 대한 lac 오페론의 수학적 모델을 구축하고, 모델이 보이는 이중안정성(바이스토빌리티) 범위를 조절하는 두 가지 핵심 파라미터를 규명하였다. 인공 유도제에서는 파라미터 조정으로 실험적으로 관찰된 이중안정성 영역을 재현할 수 있었지만, 락토스에 대해서는 생리학적으로 타당한 파라미터 범위 내에서는 이중안정성이 사라짐을 예측한다.
상세 분석
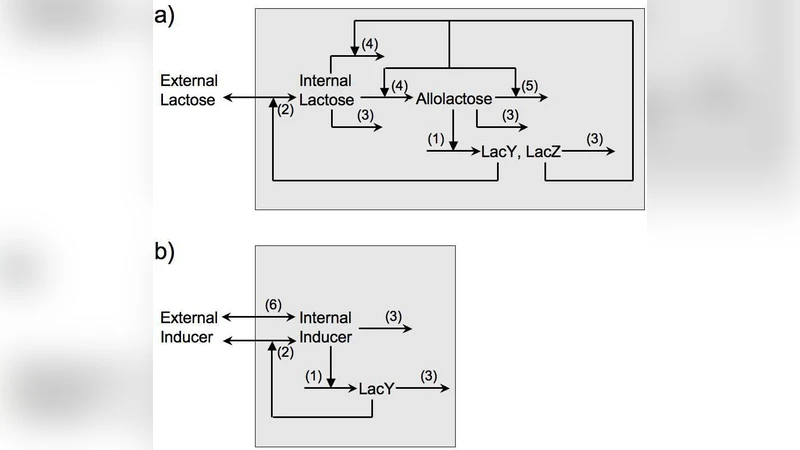
이 논문은 lac 오페론의 전사 조절을 미분방정식 형태로 정형화하고, 정적 평형 상태에서의 유도 반응을 수치적으로 탐색한다. 인공 유도제(예: IPTG, TMG)의 경우, 모델은 두 개의 ‘bistability parameters’를 도입한다. 첫 번째는 퍼미아제에 의한 유도제 흡수율과 수동 확산율의 비율이며, 두 번째는 퍼미아제에 의한 유도제 배출(역수송) 효율이다. 이 두 파라미터를 변동시키면, 유도제 농도에 대한 시스템의 응답 곡선이 S자 형태를 유지하거나 단일 안정 상태로 전이하는 임계점이 이동한다. 특히, 퍼미아제 의존 배출이 충분히 크게 되면, 내부 유도제 농도가 급격히 감소해 양극성과 음극성 두 상태가 동시에 존재할 수 있는 구간이 사라진다. 이는 IPTG와 같은 비대사성 유도제에 비해, IPTG가 세포 내에서 거의 배출되지 않음에도 불구하고, 수동 확산이 지배적인 경우(예: 높은 온도나 막 투과성 증가)에도 이중안정성이 소멸될 수 있음을 시사한다.
락토스 유도에 대해서는 모델을 확장하여, 락토스가 β-갈락토시다아제에 의해 알롤락토스로 전환되고, 알롤락토스가 lac 오페론의 전사 억제제인 LacI에 결합해 유도를 일으키는 과정을 포함한다. 여기서는 퍼미아제에 의한 락토스 흡수와 알롤락토스의 퍼미아제 의존 배출을 모두 고려한다. 파라미터 값을 실험적으로 측정된 범위(예: 퍼미아제 Km, Vmax, 세포 내 알롤락토스 분해 속도 등) 내에서 시뮬레이션하면, 유도제 농도와 내부 알롤락토스 농도 사이에 비선형적인 피드백이 존재하지만, 양극성 상태가 동시에 존재할 정도의 충분한 비선형성이 발생하지 않는다. 즉, 락토스에 대한 모델은 단일 안정 상태만을 예측한다. 다만, 퍼미아제 의존 배출 효과를 인위적으로 매우 낮게 설정하면, 제한된 파라미터 영역에서 작은 폭의 이중안정성이 나타날 수 있다. 이러한 ‘비생리학적’ 조건은 실제 세포에서 관찰되기 어렵다.
결과적으로, 논문은 두 가지 중요한 결론을 도출한다. 첫째, 인공 유도제 시스템에서는 퍼미아제 매개 수송과 수동 확산/배출의 상대적 비율을 조절함으로써 이중안정성의 존재와 범위를 정밀하게 제어할 수 있다. 둘째, 자연적인 유도제인 락토스에 대해서는, 생리학적으로 타당한 매개변수 범위 내에서는 이중안정성이 실질적으로 존재하지 않으며, 따라서 lac 오페론이 자연 환경에서 이중안정성을 이용한다는 기존 가설에 의문을 제기한다. 저자들은 이러한 모델 예측을 검증하기 위해, 퍼미아제 발현량을 인위적으로 조절하거나, 배출 효율을 억제하는 돌연변이주를 이용한 실험적 접근을 제안한다.
댓글 및 학술 토론
Loading comments...
의견 남기기