C5 도메인 접힘과 돌연변이 특성의 계산 분석
초록
Myosin Binding Protein C의 C5 도메인에 대해 원위 중심 모델을 이용한 열접힘 분자동역학 시뮬레이션을 수행하였다. 세 가지 FHC 관련 변이(N755, R654, R668)의 접힘 온도 변화와 Φ‑값 분포를 분석한 결과, N755 변이가 가장 큰 온도 감소를 일으키며 CFGA′ β‑시트의 고Φ‑값 부위에 위치함을 확인했다. 반면 R654와 R668은 낮은 Φ‑값을 가진 BDE β‑시트에 존재해 접힘 안정성에 미치는 영향이 미미하고, 주된 병리적 효과는 리간드 결합에 기인할 가능성이 있다. 또한 CD‑루프의 서열 특성을 bioinformatic 분석하여 음전하 밀도는 높고 소수성은 낮은, 본질적으로 무질서한 특성을 지닌 것으로 밝혀졌다.
상세 분석
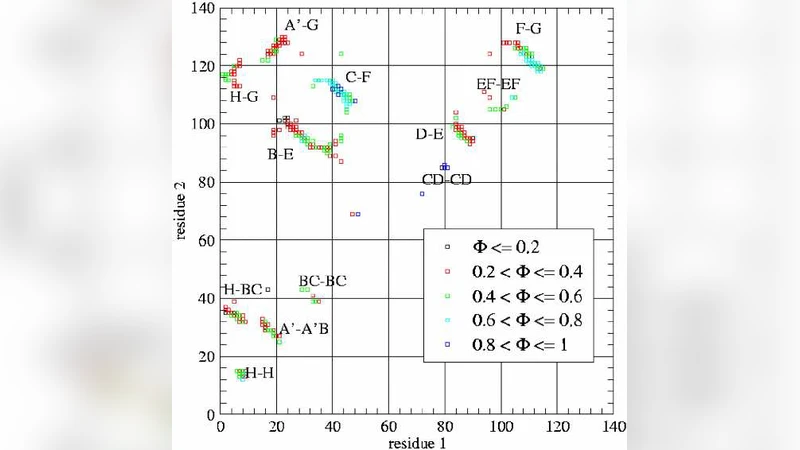
본 연구는 Myosin Binding Protein C (MyBP‑C)의 C5 도메인을 대상으로, 원위 중심(native‑centric) 포텐셜을 적용한 온도 구배(thermal‑gradient) 분자동역학 시뮬레이션을 수행함으로써, 도메인의 열역학적 접힘 특성과 세 가지 병리학적 변이(Asn755→X, Arg654→X, Arg668→X)의 구조‑기능적 영향을 정량적으로 평가하였다. 시뮬레이션 결과, Asn755 변이는 접힘 전이 온도(Tm)를 약 5 °C 이상 낮추는 가장 큰 효과를 보였으며, 이 잔기는 CFGA′ β‑시트의 핵심 구조에 위치해 Φ‑값이 0.8 ~ 0.9로 매우 높았다. 높은 Φ‑값은 해당 부위가 접힘 전이(state‑transition) 동안 구조적 형성에 크게 기여함을 의미하므로, Asn755의 친수성 손실은 전반적인 열안정성을 크게 저하시켜 실험적으로 보고된 변성(denaturation) 경향과 일치한다. 반면 Arg654와 Arg668은 각각 BDE β‑시트에 위치하며 Φ‑값이 0.2 ~ 0.3 수준으로 낮다. 이들 잔기의 변이는 Tm 변동이 0.5 °C 미만에 그쳐 접힘 과정 자체에는 거의 영향을 미치지 않는다. 따라서 병리적 메커니즘은 접힘 안정성보다는 이들 잔기가 담당하는 잠재적 리간드 결합 부위, 특히 근섬유의 actin‑myosin 복합체와의 상호작용에 기인할 가능성이 크다. 추가적으로, CD‑루프는 다른 Ig‑like 도메인에 비해 길이가 길고, 전하 분석 결과 Asp/Glu 등 음전하 잔기가 45 % 이상을 차지하며, Kyte‑Doolittle 소수성 지수는 평균 −1.2로 낮았다. 이러한 서열 특성은 CD‑루프가 본질적으로 natively unfolded 상태이며, 환경에 따라 구조적 유연성을 보이며 파트너 단백질과의 결합에 따라 접힘이 촉진될 수 있음을 시사한다. 전체적으로, 원위 중심 모델은 변이의 열역학적 효과와 구조적 위치를 정밀히 매핑함으로써, 변이가 직접적인 접힘 장애를 일으키는 경우와 기능적 결합 장애를 일으키는 경우를 구분하는 강력한 도구임을 입증하였다.
댓글 및 학술 토론
Loading comments...
의견 남기기