폴리아크릴아마이드 겔에서 단백질 은 염색
초록
은 염색은 폴리아크릴아마이드 겔에서 전기영동된 단백질을 저나노그램 수준까지 검출할 수 있는 고감도 방법이다. 고정, 감작, 은 침투, 현상 네 단계로 진행되며, 2시간에서 1일 이내에 완료할 수 있다. 염색 후에도 질량분석 등 다운스트림 분석에 적합하고, 색상은 몇 주간 안정적으로 유지된다.
상세 분석
본 논문은 은 염색의 전반적인 워크플로우와 변형 프로토콜을 체계적으로 정리한다. 첫 번째 단계인 단백질 고정은 메탄올·아세톤·포름산 혼합 용액을 사용해 겔 내 단백질을 고정함으로써 탈착을 방지하고, 이후 감작 단계에서는 나트륨 티오시안산염(Na₂S₂O₃)이나 포름산을 첨가해 은 이온의 친화성을 높인다. 감작은 은 이온이 단백질에 선택적으로 결합하도록 돕는 핵심 과정이며, 이때 pH와 온도 조절이 민감하게 작용한다. 은 침투 단계에서는 은 질산염 용액을 겔에 흡수시켜 은 이온을 충분히 공급한다. 현상 단계에서는 포름산·아스코르브산·탄산수소나트륨 혼합 용액을 사용해 은 이온을 금속 은으로 환원시켜 가시적인 밴드를 형성한다. 현상 시간은 과다 현상으로 인한 배경 증가를 방지하기 위해 정밀하게 제어해야 한다.
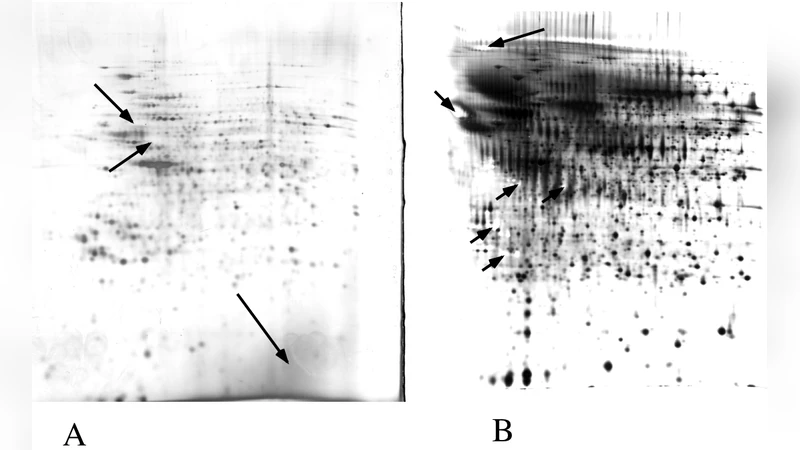
다양한 변형 프로토콜이 제시되는데, 예를 들어 글루타르알데히드·포름알데히드 혼합 고정법은 단백질 구조를 보다 보존하면서도 감작 효율을 높인다. 또한, 나트륨 초산염을 이용한 저온 현상법은 배경을 최소화하고 민감도를 0.5 ng 수준까지 끌어올린다. 이러한 변형은 실험실 환경, 겔 종류(예: SDS‑PAGE vs. 2‑D 겔), 그리고 후속 분석(예: MALDI‑TOF MS, LC‑MS/MS) 요구에 따라 선택될 수 있다.
논문은 은 염색이 질량분석에 미치는 영향을 상세히 논의한다. 은 입자가 단백질 펩타이드에 결합하면 이온화 효율이 저하될 수 있으나, 은을 제거하는 포스트‑스트립 처리(예: 포름산·시트르산 용액)나 은‑염색 후 직접적인 인-젤 소화가 가능함을 보여준다. 따라서 은 염색은 고감도 검출과 동시에 다운스트림 분석 호환성을 유지할 수 있는 실용적인 방법으로 평가된다.
마지막으로, 염색 후 색상 안정성에 대한 데이터가 제시된다. 은 염색된 겔은 실온에서 4주 이상 색이 변하지 않으며, 어두운 환경에서 보관할 경우 8주 이상 유지된다. 이는 장기 보관이나 논문용 이미지 제작에 유리하다. 전체적으로 본 논문은 은 염색의 원리, 단계별 최적화 파라미터, 변형 프로토콜, 그리고 응용 가능성을 포괄적으로 제공함으로써 연구자들이 실험 설계 시 신뢰할 수 있는 지침을 제공한다.
댓글 및 학술 토론
Loading comments...
의견 남기기